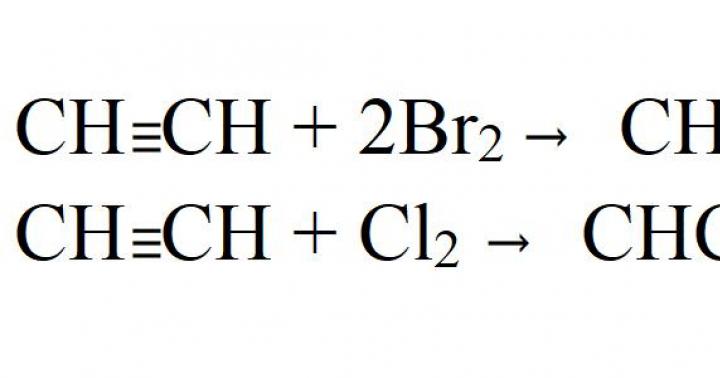ОПРЕДЕЛЕНИЕ
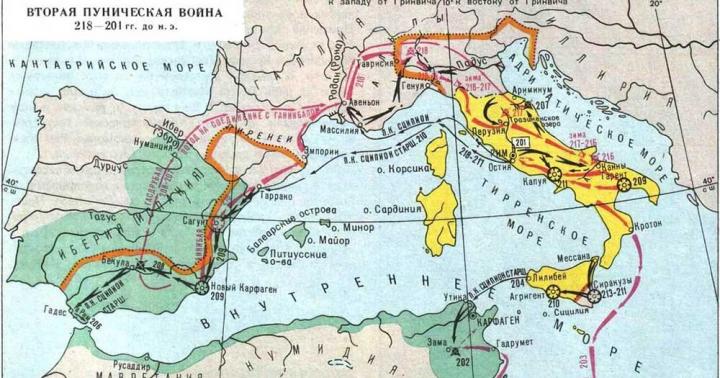
Ацетилен (этин) - газ без цвета и запаха, обладает слабым наркотическим действием (строение молекулы показано на рис. 1).
Мало растворим в воде и очень хорошо в ацетоне. В виде ацетонового раствора его хранят в стальных баллонах, заполненных каким-нибудь инертным пористым материалом. Смеси ацетилена с воздухом взрывоопасны.
Рис. 1. Строение молекулы ацетилена.
Таблица 1. Физические свойства ацетилена.
Получение ацетилена
Выделяют промышленные и лабораторные способы получения ацетилена. Так, в промышленности ацетилен получают путем высокотемпературного крекинга метана:
2CH 4 → СH≡CH +3H 2 .
В лаборатории ацетилен получают гидролизом карбида кальция:
CaC 2 +2H 2 O = Ca(OH) 2 + C 2 H 2 .
Кроме вышеперечисленных реакций, для получения ацетилена используют реакции дегидрирования алканов и алкенов:
CH 3 -CH 3 → СH≡CH +2H 2 ;
CH 2 =CH 2 → СH≡CH +H 2 .
Химические свойства ацетилена
Ацетилен вступает в реакции присоединения, протекающие по нуклеофильному механизму, такие как:
— гидрирование
СH≡CH +H 2 O→ → CH 3 -CH=O (H 2 SO 4 (18%), t = 90 o C);
— галогенирование
СH≡CH +Br 2 →CHBr=CHBr + Br 2 →CHBr 2 -CHBr 2 ;
— гидрогалогенирование
СH≡CH +HСl→ CH 2 =CHCl + HCl → CH 3 -CHCl 2 .
Кроме этого ацетилен способен образовывать соли при взаимодействии с активными металлами (1) и оксидом серебра (2):
2СH≡CH +2Na→2 СH≡C-Na + H 2 (1);
СH≡CH + Ag 2 O→ Ag- С≡C-Ag↓ + H 2 O (2).
Он способен тримеризоваться:
3C 2 H 2 → C 6 H 6 (t = 600 o C, kat = C active).
Применение ацетилена
Ацетилен является исходным продуктом для многих важнейших химических производств. Например, из ацетилена получают различные галогенпроизводные, такие как тетрахлорэтан и трихлорэтилен, являющиеся хорошими растворителями, а также винилхлорид, служащий мономером для получения поливинилхлорида. Кроме этого ацетилен используется для получения синтетических каучуков.
Примеры решения задач
ПРИМЕР 1
| Задание | Эквимолекулярная смесь ацетилена и формальдегида полностью реагирует с 69,6 г Ag 2 O, растворенного в аммиаке. Определите состав исходной смеси. |
| Решение | Запишем уравнения реакций, указанных в условии задачи:
HC≡CH + Ag 2 O → AgC≡Cag + H 2 O (1); H-C(O)H + 2 Ag 2 O → CO 2 + H 2 O + 4Ag (2). Рассчитаем количество вещества оксида серебра (I): n(Ag 2 O) = m(Ag 2 O) / M(Ag 2 O); M(Ag 2 O) = 232 г/моль; n(Ag 2 O) = 69,6 / 232 = 0,3 моль. По уравнению (2) количество вещества формальдегида будет равно 0,1 моль. По условию задачи смесь эквимолекулярна, следовательно, ацетилена тоже будет 0,1 моль. Найдем массы веществ, составляющих смесь: M(HC≡CH) = 26 г/моль; M(H-C(O)H) = 30 г/моль; m(HC≡CH) = 0,1 × 26 = 2,6 г; m(H-C(O)H) = 0,1 × 30 = 3 г. |
| Ответ | Масса ацетилена равна 2,6 г, формальдегида - 3 г. |
ПРИМЕР 2
| Задание | При пропускании смеси пропана и ацетилена через склянку с бромной водой масса склянки увеличилась на 1,3 г. При полном сгорании такого же количества исходной смеси углеводородов выделилось 14 л (н.у.) оксида углерода (IV). Определите массовую долю пропана в исходной смеси. |
| Решение | При пропускании смеси пропана и ацетилена через склянку с бромной водой происходит поглощение ацетилена. Запишем уравнение химической реакции, соответствующее этому процессу:
НC ≡ СH + 2Вr 2 → НСВr 2 -СНВr 2 . Таким образом, значение, на которое увеличилась масса склянки (1,3 г) представляет собой массу ацетилена. Найдем количество вещества ацетилена (молярная масса - 26 г/моль): n (C 2 H 2) = m (C 2 H 2) / M (C 2 H 2); n (C 2 H 2) = 1,3/26 = 0,05 моль. Запишем уравнение реакции сгоранияацетилена: 2С 2 Н 2 + 5О 2 = 4СО 2 + 2Н 2 О. Согласно уравнению реакции, в неё вступило 2 моль ацетилена, однако, известно, что 0,05 моль из этого количества поглотилось бромной водой. Т.е. выделилось: 2-0,05 = 0,1 моль СО 2 . Найдем общее количество оксида углерода (IV): n sum (CO 2) = V (CO 2) / V m ; n sum (CO 2) = 14/22,4 = 0,625 моль. Запишем уравнение реакции сгорания пропана: С 3 Н 8 + 5О 2 = 3СO 2 + 4Н 2 О. Учитывая, что в реакции сгорания ацетилена выделилось 0,1 моль оксида углерода (IV), количество вещества оксида углерода (IV), выделившееся в ходе сгорания пропана равно: 0,625 — 0,1 = 0,525 моль СО 2 . Найдем количество вещества пропана, вступившего в реакцию горения. Согласно уравнению реакции n(CO 2) : n(С 3 Н 8) = 3: 1, т.е. n(С 3 Н 8) = n(CO 2) / 3 = 0,525/3 = 0,175 моль. Вычислим массу пропана (молярная масса 44 г/моль): m(С 3 Н 8) = n(С 3 Н 8) ×M(С 3 Н 8); m(С 3 Н 8) = 0,175 × 44 = 7,7 г. Тогда, общая масса смеси углеводородов составит: m mixture = m(C 2 H 2) + m(С 3 Н 8) = 1,3+7,7 = 9,0 г. Найдем массовую долю пропана в смеси: ω = m / m mixture × 100%; ω(С 3 Н 8) = m(С 3 Н 8) / m mixture × 100%; ω(С 3 Н 8) =7,7/9,0× 100% = 0,856 × 100%= 85,6%. |
| Ответ | Массовая доля пропана 85,6%. |
Ацетилен (или по международной номенклатуре - этин) - это непредельный углеводород, принадлежащий к классу алкинов. Химическая формула ацетилена - C2H2. Атомы углерода в молекуле соединены тройной связью. Он является первым в своем гомологическом ряду. Представляет собой бесцветный газ. Очень огнеопасен.
Получение
Все методы промышленного получения ацетилена сходятся к двум типам: гидролиз карбида кальция и пиролиз различных углеводородов. Последний требует меньших энергозатрат, но чистота продукта довольно низкая. У карбидного метода - наоборот.
Суть пиролиза заключается в том, что метан, этан или другой легкий углеводород при нагреве до высоких температур (от 1000 °C) превращается в ацетилен с выделением водорода. Нагрев может осуществятся электрическим разрядом, плазмой или сжиганием части сырья. Но проблема состоит в том, что в результате реакции пиролиза может образовываться не только ацетилен, но и еще множество разных продуктов, от которых необходимо впоследствии избавляться.
2CH4 → C2H2 + 3H2
Карбидный метод основан на реакции взаимодействия карбида кальция с водой. Карбид кальция получают из его оксида, сплавляя с коксом в электропечах. Отсюда и такой высокий расход энергии. Зато чистота ацетилена, получаемого таким способом, крайне высока (99,9 %).
CaC2 + H2O → C2H2 + Ca(OH)2
В лаборатории ацетилен также можно получить дегидрогалогенированием дигалогенпроизводных алканов с помощью спиртового раствора щелочи.
CH2Cl-CH2Cl + 2KOH → C2H2 + 2KCl + 2H2O
Физические свойства ацетилена
Ацетилен - это газ без цвета и запаха. Хотя примеси могут давать ему чесночный запах. Практически не растворим в воде, немного растворим в ацетоне. При температуре -83,8 °C сжижается.
Химические свойства ацетилена
Исходя из тройной связи ацетилена, для него будут характерны реакции присоединения и реакции полимеризации. Атомы водорода в молекуле ацетилена могут замещаться другими атомами или группами. Поэтому можно сказать, что ацетилен проявляет кислотные свойства. Разберем химические свойства ацетилена на конкретных реакциях.
Реакции присоединения:
- Гидрирование. Осуществляется при высокой температуре и в присутствии катализатора (Ni, Pt, Pd). На палладиевом катализаторе возможно неполное гидрирование.
- Галогенирование. Может быть как частичным, так и полным. Идет легко даже без катализаторов или нагревания. На свету хлорирование идет с взрывом. При этом ацетилен полностью распадается до углерода.

- Присоединение к уксусной кислоте и этиловому спирту. Реакции идут только в присутствии катализаторов.

- Присоединение синильной кислоты.
CH≡CH + HCN → CH2=CH-CN
Реакции замещения:
- Взаимодействие ацетилена с металл-органическими соединениями.
CH≡CH + 2C2H5MgBr → 2C2H6 + BrMgC≡CMgBr
- Взаимодействие с металлическим натрием. Необходима температура 150 °C или предварительное растворение натрия в аммиаке.
2CH≡CH + 2Na → 2CH≡CNa + H2
- Взаимодействие с комплексными солями меди и серебра.

- Взаимодействие с амидом натрия.
CH≡CH + 2NaNH2 → NaC≡CNa + 2NH3
Реакции полимеризации:
- Димеризация. При этой реакции две молекулы ацетилена объединяются в одну. Необходим катализатор - соль одновалентной меди.
- Тримеризация. В этой реакции три молекулы ацетилена образуют бензол. Необходим нагрев до 70 °C, давление и катализатор.
- Тетрамеризация. В результате реакции получается восьмичленный цикл - циклооктатетраен. Для этой реакции также требуется небольшой нагрев, давление и соответствующий катализатор. Обычно это комплексные соединения двухвалентного никеля.

Это далеко не все химические свойства ацетилена.
Применение
Структурная формула ацетилена указывает нам на довольно прочную связь между атомами углерода. При ее разрыве, например при горении, выделяется очень много энергии. По этой причине ацетиленовое пламя обладает рекордно высокой температурой - около 4000 °C. Его используют в горелках для сварки и резки металла, а также в ракетных двигателях.
Пламя горения ацетилена имеет также очень высокую яркость, поэтому его часто используют в осветительных приборах. Используется он и во взрывотехнике. Правда, там применяется не сам ацетилен, а его соли.
Как видно из разнообразных химический свойств, ацетилен может применяться как сырье для синтеза других важных веществ: растворителей, лаков, полимеров, синтетических волокон, пластмасс, органического стекла, взрывчатых веществ и уксусной кислоты.
Безопасность
Как уже говорилось, ацетилен - огнеопасное вещество. С кислородом или воздухом он способен образовывать крайне легковоспламеняющиеся смеси. Чтобы вызвать взрыв, достаточно одной искры от статического электричества, нагрева до 500 °C или небольшого давления. При температуре 335 °C чистый ацетилен самовоспламеняется.
Из-за этого ацетилен хранят в баллонах под давлением, которые наполнены пористым веществом (пемза, активированный уголь, асбест). Таким образом, ацетилен распределяется по порам, уменьшая риск взрыва. Часто эти поры пропитывают ацетоном, из-за чего образуется раствор ацетилена. Иногда ацетилен разбавляют другими, более инертными газами (азот, метан, пропан).
Этот газ обладает и токсичным действием. При его вдыхании начнется интоксикация организма. Признаками отравления являются тошнота, рвота, шум в ушах, головокружение. Большие концентрации могут приводить даже к потере сознания.
Введение
Ацетилен (C 2 H 2) – химическое газообразное соединение углерода с водородом, без цвета, со слабым эфирным запахом и сладковатым вкусом.
Ацетилен в газосварочном производстве получил наибольшее распространение благодаря важным для сварки качествам (высокая температура пламени, большая теплота сгорания). Так, при разложении 1 кг ацетилена выделяется 8473,6 кДж теплоты. Это единственный газ, горение которого возможно при отсутствии кислорода (или окислителя вообще).
Выделение тепла при сгорании ацетилена обусловлено следующими процессами:
- распад ацетилена: C 2 H 2 = 2C + H 2
- сгорание углерода: 2С + O 2 = 2CO, 2CO + O 2 = 2CO 2
- сгорание водорода: H 2 + 1/2O 2 = H 2 O
Ацетилен легче воздуха, масса 1 м 3 ацетилена при температуре 20 °С (273 К) и нормальном атмосферном давлении составляет 1,09 кг. При нормальном давлении и температуре от –82,4 °С (190,6 К) до –84,0 °С (189 К) ацетилен переходит в жидкое состояние, а при температуре –85 °С (188 К) затвердевает, образуя кристаллы.
Технический ацетилен выпускается двух видов: растворенный и газообразный.
Технический растворенный ацетилен марки А предназначается для питания осветительных установок, технический растворенный ацетилен марки Б и технический газообразный ацетилен предназначаются в качестве горючего газа при газопламенной обработке металлов.
Технический ацетилен получают из карбида кальция путем разложения последнего водой. При этом из карбида кальция в ацетилен переходят вредные примеси, загрязняющие ацетилен: сероводород, аммиак, фосфорный водород, кремнистый водород. Эти примеси могут ухудшать свойства наплавленного металла и поэтому удаляются из ацетилена промывкой в воде и химической очисткой. Особенно нежелательна примесь фосфористого водорода, содержание более 0,7 % в ацетилене повышает взрывоопасность последнего.
Свойства ацетилена
Основные свойства ацетилена приведены в таблице 1.
| Показатель | Данные показателя |
|---|---|
| Формула | С 2 H 2 |
| Молекулярная масса | 26,038 |
| Плотность (при 0 °С и давлении 760 мм рт. ст.), кг/м 3 | 1,17 |
| Плотность (при 20 °С и давлении 760 мм рт. ст.), кг/м 3 | 1,09 |
| Критическая температура, °С | 35,9 |
| Критическое давление, кгс/см 2 | 61,6 |
| Температура пламени, °С | 3150-3200 |
| Температура кипения (при 760 мм рт. ст.), °С | -81,8 |
| Температура плавления (затвердевания) (при 760 мм рт. ст.), °С | -85 |
| Высшая удельная теплота сгорания, кДж/м 3 | 58660 |
| Низшая удельная теплота сгорания, кДж/м 3 | 55890 |
| Температура самовоспламенения, °С | 335 |
| Давление самовоспламенения, МПа | 0,14–0,16 |
По физико-химическим показателям технический ацетилен должен соответствовать нормам, указанным в таблице 2.
| Показатель | Для ацетилена | |||
|---|---|---|---|---|
| растворенного | газообразного | |||
| марки А | марки Б | |||
| высшей категории качества | высшей категории качества | первой категории качества | ||
| Объемная доля ацетилена, % не менее | 99,5 | 99,1 | 98,8 | 98,5 |
| Объемная доля воздуха и других малорастворимых в воде газов, % не более | 0,5 | 0,8 | 1,0 | 1,4 |
| Объемная доля фосфористого водорода, % не более | 0,005 | 0,02 | 0,05 | 0,08 |
| Объемная доля сероводорода, % не более | 0,002 | 0,005 | 0,05 | 0,05 |
| Массовая концентрация водяных паров при температуре 20 °С и давлении 101,3 кПа (760 мм рт. ст.), г/м 3 , не более Что соответствует температуре насыщения, °С, не выше |
0,4 | 0,5 | 0,6 | Не нормируется |
Растворимость ацетилена
Газообразный ацетилен может растворятся во многих жидкостях. Данные о растворимости ацетилена в некоторых жидкостях при атмосферном давлении и температуре 15 °С приведены в таблице 3.
Растворимость ацетилена в жидкостях с понижением температуры увеличивается. Данные о растворимости ацетилена в ацетоне при различных температурах приведены в таблице 4.
Растворенным ацетиленом называется ацетилен, находящийся в баллоне, заполненном пористой массой, пропитанной растворителем – ацетоном. Искусственное охлаждение баллонов ускоряет процесс их наполнения. В порах пористой массы ацетилен растворен в ацетоне. При открывании вентиля баллона ацетилен выделяется из ацетона в виде газа. Растворенный ацетилен предназначен для его хранения и транспортирования.
Взрывоопасность ацетилена
При использовании ацетилена необходимо учитывать его взрывоопасные свойства. Это единственный широко применяемый в промышленности газ, горение и взрыв которого возможны даже при отсутствии кислорода или других окислителей.
Температура самовоспламенения ацетилена зависит от давления (таблица 5).
Повышение давления существенно уменьшает температуру самовоспламенения ацетилена. Частицы других веществ, присутствующие в ацетилене, увеличивают поверхность его контакта и тем самым снижают температуру самовоспламенения при атмосферном давлении до следующих значений, °С (К):
- железная стружка – 520 (793);
- латунная стружка – 500–520 (773–793);
- карбид кальция – 500 (773);
- оксид алюминия – 490 (763);
- медная стружка – 460 (733);
- активированный уголь – 400 (673);
- гидрат оксида железа (ржавчина) – 280–300 (553–573);
- оксид железа – 280 (553);
- оксид меди – 250 (523).
Если ацетилен медленно нагревать до температуры 700–800 °С (973–1073 К) при атмосферном давлении, то происходит его полимеризация, при которой молекулы уплотняются и образуют более сложные соединения: бензол C 6 H 6 , стирол C 8 H 8 , нафталин C 10 H 8 , толуол C 7 H 8 и др. Полимеризация всегда сопровождается выделением теплоты и при быстром нагреве ацетилена может перейти в его самовоспламенение или взрывчатый распад.
Если при сжатии ацетилена в компрессоре до давления 29 кгс/м 3 (2,9 МПа) температура при завершении этого процесса не превышает 275 °С (548 К), то воспламенения не происходит, что позволяет наполнять баллоны ацетоном с целью его длительного хранения и транспортирования. С повышением давления температура, при которой начинается процесс полимеризации, понижается (рис.1).
При практическом использовании ацетилена допустим его нагрев до следующих значений температуры, °С (К):
- 300 (573) – при давлении 1 кгс/см 2 (0,1 МПа);
- 150–180 (423–453) – при 2,5 кгс/см 2 (0,25 МПа);
- 100 (373) – при более высоких давлениях.
Одним из важных показателей взрывоопасности горючих газов и паров является энергия зажигания. Чем меньше эта величина, тем взрывоопаснее данной вещество. Значения энергии зажигания ацетилена (при нормальных условиях): с воздухом – 19 кДж; в кислородом – 0,3 кДж.
Водяной пар служит флегматизатором для ацетилена, т.е. его присутствие существенно снижает способность ацетилена к самовоспламенению при наличии случайных источников теплоты и взрывчатому распаду. Согласно действующим нормам для ацетиленовых генераторов, в которых ацетилен всегда насыщен парами воды, предельное избыточное давление составляет 150 кПа, а абсолютное – 250 кПа.
При атмосферном давлении смесь ацетилена с воздухом взрывоопасна, если в ней содержатся 2,2 % ацетилена и более, смесь с кислородом – 2,8 % ацетилена и более (верхних пределов концентрации ацетилена для его смесей с воздухом и кислородом не существует, так как при достаточной энергии зажигания способен взрываться и чистый ацетилен).
Получение ацетилена
В промышленности ацетилен получают при разложении жидких горючих, таких как нефть, керосин, воздействием электродугового разряда. Применяется также способ производства ацетилена из природного газа (метана). Смесь метана с кислородом сжигают в специальных реакторах при температуре 1300–1500 °С. Из полученной смеси с помощью растворителя извлекается концентрированный ацетилен. Получение ацетилена промышленным способом на 30–40 % дешевле, чем из карбида калия. Промышленный ацетилен закачивается в баллоны, где находится в порах специальный массы растворенным в ацетоне. В таком виде потребители получают баллонный промышленный ацетилен. Свойства ацетилена не зависят от способа его получения. Остаточное давление в ацетиленовом баллоне при температуре 20 °С должно быть 0,05–0,1 МПа (0,5–1,0 кгс/см 2). Рабочее давление в наполненном баллоне не должно превышать 1,9 МПа (19 кгс/см 2) при 20 °С.
Для сохранности наполнительной массы нельзя отбирать ацетилен из баллона со скоростью 1700 дм 3 /ч.
Рассмотрим подробнее способ получения ацетилена в генераторе из карбида кальция. Карбид кальция получают путем сплавления кокса и негашеной извести в электрических дуговых печах при температуре 1900–2300 °С, при которой протекает реакция:
Ca + 3C = CaC 2 + CO
Расплавленный карбид кальция сливают из печи в формы-изложницы, где он остывает. Далее его дробят и сортируют на куски размером от 2 до 80 мм. Готовый карбид кальция упаковывают в герметически закрываемые кальция не должно быть более 3 % частиц размером менее 2 мм (пыль). По ГОСТу 1460-81 устанавливаются размеры (грануляция) кусков карбида кальция: 2×8; 8×15; 15×25; 25×80 мм.
При взаимодействии с водой карбид кальция выделяет газообразный ацетилен и образует в остатке гашеную известь, являющуюся отходом.
Реакция разложения карбида кальция водой происходит по схеме:
Из 1 кг химически чистого карбида кальция теоретически можно получить 372 дм 3 (литра) ацетилена. Практически из-за наличия примесей в карбиде кальция выход ацетилена составляет до 280 дм 3 (литров). В среднем для получения 1000 дм 3 (литров) ацетилена расходуется 4,3–4,5 кг карбида кальция.
Карбидная пыль при смачивании водой разлагается почти мгновенно. Карбидную пыль нельзя применять в обычных ацетиленовых генераторах, рассчитанных для работы на кусковом карбиде кальция. Для разложения карбидной пыли применяются генераторы специальной конструкции. Для охлаждения ацетилена при разложении карбида кальция. Применяют также от 5 до 20 дм 3 (литров) воды на 1 кг карбида кальция. Применяют также «сухой» способ разложения карбида кальция. На 1 кг мелко раздробленного карбида кальция в генератор подают 0,2–1 дм 3 (литра) воды. В этом процессе гашения известь получается не в виде жидкого известкового ила, а в виде сухой «пушонки», удаление, транспортировка и утилизация которой значительно упрощается.
Транспортирование и хранение
Технический газообразный ацетилен транспортируют по трубопроводам из стальных бесшовных труб по ГОСТ 8731 и ГОСТ 8734. Давление ацетилена в трубопроводе должно быть не более 0,15 МПа (1,5 кгс/см 2). Окраска трубопроводов – по ГОСТ 14202.
Давление газа в трубопроводе должно измеряться манометром класса точности 2,5 по ГОСТ 8625, на циферблате которого должна стоять надпись «Ацетилен».
Техническим растворенным ацетиленом наполняют стальные баллоны для растворенного ацетилена с пористой массой (активным углем или литой пористой массой) и ацетиленом.
Баллоны должны быть оснащены вентилями специальных типов, предназначенными для ацетиленовых баллонов.
Давление газа в баллоне должно измеряться манометром класса точности не ниже 4 по ГОСТ 8625. Температуру газа в баллоне принимают равной температуре окружающей среды, в которой наполненный баллон должен быть выдержан не менее 8 ч.
При номинальном давлении 1,9 МПа (19,0 кгс/см 2) при 20 °С давление газа в баллоне в интервале температур от минус 5 до плюс 40 °С должно соответствовать указанному в таблице 6.
| Температура газа, °С |
Давление газа в баллоне, МПа (кгс/см 2), не более |
|---|---|
| -5 | 1,34 (13,4) |
| 0 | 1,40 (14,0) |
| +5 | 1,50 (15,0) |
| +10 | 1,65 (16,5) |
| +15 | 1,80 (18,0) |
| +20 | 1,90 (19,0) |
| +25 | 2,15 (21,5) |
| +30 | 2,35 (23,5) |
| +35 | 2,60 (26,0) |
| +40 | 3,00 (30,0) |
Остаточное давление газа в баллоне измеряют манометром класса точности 2,5 диаметром шкалы не менее 100 мм по ГОСТ 8625.
Баллоны от потребителя должны поступать с остаточным давлением, соответствующим указанному в таблице 7.
Растворенный ацетилен в баллонах перевозят всеми видами транспорта в соответствии с правилами перевозки опасных грузов, действующими на данном виде транспорта, и правилами устройства и безопасной эксплуатации сосудов, работающих под давлением.
По железной дороге баллоны, наполненные растворенным ацетиленом, транспортируют повагонными и мелкими отправками в крытых вагонах. При транспортировании мелкими отправками колпаки баллонов должны быть опломбированы.
Для механизации погрузочно-разгрузочных работ и укрупнения перевозок автомобильным транспортом баллоны среднего объема помещают в металлические специальные контейнеры.
При транспортировании баллонов малого объема всеми видами транспорта они должны быть дополнительно упакованы в дощатые решетчатые ящики типа VII по ГОСТ 2991. Баллоны должны укладываться в ящики горизонтально, вентилями в одну сторону с обязательными прокладками между баллонами, предохраняющими их от ударов друг о друга.
Баллоны, наполненные ацетиленом, хранят в специальных складских помещениях или на открытых площадках под навесом, защищающим их от атмосферных осадков и прямых солнечных лучей, по группе ОЖ 2 ГОСТ 15150.
Требования безопасности
Ацетилен – взрывоопасный газ. Взрывы ацетилена обладают большой разрушительной силой.
С воздухом образует взрывоопасную смесь с нижним концентрационным пределом воспламенения при атмосферном давлении, приведенным к температуре 25 °С, – 2,5 % (по объему) по ГОСТ 12.1.004-85.
Температура самовоспламенения 335 °С.
Давление самовоспламенения 0,14–0,16 МПа.
При определенных условиях ацетилен реагирует с медью, образуя взрывоопасные соединения, поэтому категорически запрещается при изготовлении ацетиленового обо-рудования применение сплавов, содержащих более 70 % меди.
Давление, образующееся при взрыве ацетилена, зависит от начальных параметров и характера взрыва. Оно может увеличиться примерно в 10-12 раз по сравнению с начальным при взрыве в небольших сосудах и возрасти при детонации чистого ацетилена в 22 раза, а при детонации ацетилено-кислородной смеси в 50 раз.
Технический ацетилен (с примесями) имеет резкий неприятный запах; длительное вдыхание его вызывает тошноту, головокружение и даже отравление. Ацетилен обладает наркотическим действием. Отравление вызывает, главным образом, фосфористый водород, находящийся в карбидном ацетилене.
Газообразный ацетилен легче воздуха и накапливается в высших точках слабо проветриваемых помещений, где возможно образование ацетилено-воздушной смеси.
Производство ацетилена по пожарной опасности относится к категории А, по классам взрывоопасных зон – к классам В1; В1а; В1б; В1г.
Помещения ацетиленового производства должны иметь приточную и вытяжную вентиляцию.
В качестве средств пожаротушения следует использовать сжатый азот, углекислотные огнетушители, асбестовое полотно, песок.
Ацетилен (или по международной номенклатуре - этин) - это непредельный углеводород, принадлежащий к классу алкинов. Химическая формула ацетилена - C 2 H 2 . Атомы углерода в молекуле соединены тройной связью. Он является первым в своем гомологическом ряду. Представляет собой бесцветный газ. Очень огнеопасен.
Получение
Все методы промышленного получения ацетилена сходятся к двум типам: гидролиз карбида кальция и пиролиз различных углеводородов. Последний требует меньших энергозатрат, но чистота продукта довольно низкая. У карбидного метода - наоборот.
Суть пиролиза заключается в том, что метан, этан или другой легкий углеводород при нагреве до высоких температур (от 1000 °C) превращается в ацетилен с выделением водорода. Нагрев может осуществятся электрическим разрядом, плазмой или сжиганием части сырья. Но проблема состоит в том, что в результате реакции пиролиза может образовываться не только ацетилен, но и еще множество разных продуктов, от которых необходимо впоследствии избавляться.
2CH 4 → C 2 H 2 + 3H 2
Карбидный метод основан на реакции взаимодействия карбида кальция с водой. Карбид кальция получают из его оксида, сплавляя с коксом в электропечах. Отсюда и такой высокий расход энергии. Зато чистота ацетилена, получаемого таким способом, крайне высока (99,9 %).
CaC 2 + H 2 O → C 2 H 2 + Ca(OH) 2
В лаборатории ацетилен также можно получить дегидрогалогенированием дигалогенпроизводных алканов с помощью спиртового раствора щелочи.
CH 2 Cl-CH 2 Cl + 2KOH → C 2 H 2 + 2KCl + 2H 2 O
Физические свойства ацетилена
Ацетилен - это газ без цвета и запаха. Хотя примеси могут давать ему чесночный запах. Практически не растворим в воде, немного растворим в ацетоне. При температуре -83,8 °C сжижается.
Химические свойства ацетилена
Исходя из тройной связи ацетилена, для него будут характерны реакции присоединения и реакции полимеризации. Атомы водорода в молекуле ацетилена могут замещаться другими атомами или группами. Поэтому можно сказать, что ацетилен проявляет кислотные свойства. Разберем химические свойства ацетилена на конкретных реакциях.
- Гидрирование. Осуществляется при высокой температуре и в присутствии катализатора (Ni, Pt, Pd). На палладиевом катализаторе возможно неполное гидрирование.
- Галогенирование. Может быть как частичным, так и полным. Идет легко даже без катализаторов или нагревания. На свету хлорирование идет с взрывом. При этом ацетилен полностью распадается до углерода.

- Присоединение к уксусной кислоте и этиловому спирту. Реакции идут только в присутствии катализаторов.

- Присоединение синильной кислоты.
CH≡CH + HCN → CH 2 =CH-CN
Реакции замещения:
- Взаимодействие ацетилена с металл-органическими соединениями.
CH≡CH + 2C 2 H 5 MgBr → 2C 2 H 6 + BrMgC≡CMgBr
- Взаимодействие с металлическим натрием. Необходима температура 150 °C или предварительное растворение натрия в аммиаке.
2CH≡CH + 2Na → 2CH≡CNa + H 2
- Взаимодействие с комплексными солями меди и серебра.

- Взаимодействие с амидом натрия.
CH≡CH + 2NaNH 2 → NaC≡CNa + 2NH 3
- Димеризация. При этой реакции две молекулы ацетилена объединяются в одну. Необходим катализатор - соль одновалентной меди.
- Тримеризация. В этой реакции три молекулы ацетилена образуют бензол. Необходим нагрев до 70 °C, давление и катализатор.
- Тетрамеризация. В результате реакции получается восьмичленный цикл - циклооктатетраен. Для этой реакции также требуется небольшой нагрев, давление и соответствующий катализатор. Обычно это комплексные соединения двухвалентного никеля.

Это далеко не все химические свойства ацетилена.
Применение
Структурная формула ацетилена указывает нам на довольно прочную связь между атомами углерода. При ее разрыве, например при горении, выделяется очень много энергии. По этой причине ацетиленовое пламя обладает рекордно высокой температурой - около 4000 °C. Его используют в горелках для сварки и резки металла, а также в ракетных двигателях.
Пламя горения ацетилена имеет также очень высокую яркость, поэтому его часто используют в осветительных приборах. Используется он и во взрывотехнике. Правда, там применяется не сам ацетилен, а его соли.
Как видно из разнообразных химический свойств, ацетилен может применяться как сырье для синтеза других важных веществ: растворителей, лаков, полимеров, синтетических волокон, пластмасс, органического стекла, взрывчатых веществ и уксусной кислоты.
Безопасность
Как уже говорилось, ацетилен - огнеопасное вещество. С кислородом или воздухом он способен образовывать крайне легковоспламеняющиеся смеси. Чтобы вызвать взрыв, достаточно одной искры от статического электричества, нагрева до 500 °C или небольшого давления. При температуре 335 °C чистый ацетилен самовоспламеняется.
Из-за этого ацетилен хранят в баллонах под давлением, которые наполнены пористым веществом (пемза, активированный уголь, асбест). Таким образом, ацетилен распределяется по порам, уменьшая риск взрыва. Часто эти поры пропитывают ацетоном, из-за чего образуется раствор ацетилена. Иногда ацетилен разбавляют другими, более инертными газами (азот, метан, пропан).
Этот газ обладает и токсичным действием. При его вдыхании начнется интоксикация организма. Признаками отравления являются тошнота, рвота, шум в ушах, головокружение. Большие концентрации могут приводить даже к потере сознания.
Получение
В лаборатории
В лаборатории, а также в газосварочном оборудовании, ацетилен получают действием воды на карбид кальция (Ф. Вёлер , 1862 год),
Получаемый ацетилен имеет высокую степень чистоты 99,9 %. Основным недостатком процесса является высокий расход электроэнергии: 10000-11000 кВт ч на 1 тонну ацетилена.
Физические свойства
Ацетилен требует большой осторожности при обращении. Может взрываться от удара, при нагреве до 500 °C или при сжатии выше 0,2 МПа при комнатной температуре. Струя ацетилена, выпущенная на открытый воздух , может загореться от малейшей искры, в том числе от разряда статического электричества с пальца руки. Для хранения ацетилена используются специальные баллоны, заполненные пористым материалом, пропитанным ацетоном .
Химические свойства
 Для ацетилена (этина) характерны реакции присоединения:
Для ацетилена (этина) характерны реакции присоединения:
HC≡CH + Cl 2 -> ClCH=СНСl
Ацетилен с водой, в присутствии солей и других катализаторов , образует уксусный альдегид (реакция Кучерова). В силу наличия тройной связи, молекула высокоэнергетична и обладает большой удельной теплотой сгорания - 14000 ккал/м³ (50,4 МДж/кг). При сгорании в кислороде температура пламени достигает 3150 °C. Ацетилен может полимеризироваться в бензол и другие органические соединения (полиацетилен , винилацетилен). Для полимеризации в бензол необходим графит и температура в ~500 °C. В присутствии катализаторов, например, трикарбонил(трифенилфосфин)никеля, температуру реакции циклизации можно снизить до 60-70 °C.
Основные химические реакции ацетилена (реакции присоединения, сводная таблица 1.) :

Основные химические реакции ацетилена (реакции присоединения, димеризации, полимеризации, цикломеризации, сводная таблица 2.) :

Реагирует с аммиачными растворами солей Cu(I) и Ag(I) с образованием малорастворимых, взрывчатых ацетиленидов - эта реакция используется для качественного определения ацетилена и его отличия от алкенов (которые тоже обесцвечивают бромную воду и раствор перманганата калия).
История
Применение
 Ацетилен используют:
Ацетилен используют:
Безопасность
Поскольку ацетилен нерастворим в воде, и его смеси с кислородом могут взрываться в очень широком диапазоне концентраций, его нельзя собирать в газометры.
Ацетилен взрывается при температуре около 500 °C или давлении выше 0,2 МПа; КПВ 2,3-80,7 %, температура самовоспламенения 335 °C. Взрывоопасность уменьшается при разбавлении ацетилена другими газами, например азотом , метаном или пропаном .
При длительном соприкосновении ацетилена с медью и серебром образуются ацетилениды меди и серебра, которые взрываются при ударе или повышении температуры. Поэтому при хранении ацетилена не используются материалы, содержащие медь (например, вентили баллонов).
Ацетилен обладает незначительным токсическим действием. Для ацетилена нормирован ПДКм.р. = ПДК с.с. = 1,5 мг/м³ согласно гигиеническим нормативам ГН 2.1.6.1338-03 «Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населённых мест».
ПДКр.з. (рабочей зоны) не установлен (по ГОСТ 5457-75 и ГН 2.2.5.1314-03), так как концентрационные пределы распределения пламени в смеси с воздухом составляет 2,5-100 %.
Хранят и перевозят его в заполненных инертной пористой массой (например, древесным углём) стальных баллонах белого цвета (с красной надписью «А») в виде раствора в ацетоне под давлением 1,5-2,5 МПа.
Напишите отзыв о статье "Ацетилен"
Примечания
Литература
- Миллер С. А. Ацетилен, его свойства, получение и применение. - Л. : Химия, 1969. - Т. 1. - 680 с.
- Корольченко А. Я., Корольченко Д. А. Пожаровзрывоопасность веществ и материалов и средства их тушения. Справочник: в 2-х частях. Часть 1. - М .: Ассоциация «Пожнаука», 2004. - 713 с. - ISBN 5-901283-02-3 .
Ссылки
- // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). - СПб. , 1890-1907.
|
||||||||||||||||||||||||||||||||||
Отрывок, характеризующий Ацетилен
– Ты подожди лучше, когда замуж выйдет…– Ты знаешь, – сказал Анатоль, – j"adore les petites filles: [обожаю девочек:] – сейчас потеряется.
– Ты уж попался раз на petite fille [девочке], – сказал Долохов, знавший про женитьбу Анатоля. – Смотри!
– Ну уж два раза нельзя! А? – сказал Анатоль, добродушно смеясь.
Следующий после театра день Ростовы никуда не ездили и никто не приезжал к ним. Марья Дмитриевна о чем то, скрывая от Наташи, переговаривалась с ее отцом. Наташа догадывалась, что они говорили о старом князе и что то придумывали, и ее беспокоило и оскорбляло это. Она всякую минуту ждала князя Андрея, и два раза в этот день посылала дворника на Вздвиженку узнавать, не приехал ли он. Он не приезжал. Ей было теперь тяжеле, чем первые дни своего приезда. К нетерпению и грусти ее о нем присоединились неприятное воспоминание о свидании с княжной Марьей и с старым князем, и страх и беспокойство, которым она не знала причины. Ей всё казалось, что или он никогда не приедет, или что прежде, чем он приедет, с ней случится что нибудь. Она не могла, как прежде, спокойно и продолжительно, одна сама с собой думать о нем. Как только она начинала думать о нем, к воспоминанию о нем присоединялось воспоминание о старом князе, о княжне Марье и о последнем спектакле, и о Курагине. Ей опять представлялся вопрос, не виновата ли она, не нарушена ли уже ее верность князю Андрею, и опять она заставала себя до малейших подробностей воспоминающею каждое слово, каждый жест, каждый оттенок игры выражения на лице этого человека, умевшего возбудить в ней непонятное для нее и страшное чувство. На взгляд домашних, Наташа казалась оживленнее обыкновенного, но она далеко была не так спокойна и счастлива, как была прежде.
В воскресение утром Марья Дмитриевна пригласила своих гостей к обедни в свой приход Успенья на Могильцах.
– Я этих модных церквей не люблю, – говорила она, видимо гордясь своим свободомыслием. – Везде Бог один. Поп у нас прекрасный, служит прилично, так это благородно, и дьякон тоже. Разве от этого святость какая, что концерты на клиросе поют? Не люблю, одно баловство!
Марья Дмитриевна любила воскресные дни и умела праздновать их. Дом ее бывал весь вымыт и вычищен в субботу; люди и она не работали, все были празднично разряжены, и все бывали у обедни. К господскому обеду прибавлялись кушанья, и людям давалась водка и жареный гусь или поросенок. Но ни на чем во всем доме так не бывал заметен праздник, как на широком, строгом лице Марьи Дмитриевны, в этот день принимавшем неизменяемое выражение торжественности.
Когда напились кофе после обедни, в гостиной с снятыми чехлами, Марье Дмитриевне доложили, что карета готова, и она с строгим видом, одетая в парадную шаль, в которой она делала визиты, поднялась и объявила, что едет к князю Николаю Андреевичу Болконскому, чтобы объясниться с ним насчет Наташи.
После отъезда Марьи Дмитриевны, к Ростовым приехала модистка от мадам Шальме, и Наташа, затворив дверь в соседней с гостиной комнате, очень довольная развлечением, занялась примериваньем новых платьев. В то время как она, надев сметанный на живую нитку еще без рукавов лиф и загибая голову, гляделась в зеркало, как сидит спинка, она услыхала в гостиной оживленные звуки голоса отца и другого, женского голоса, который заставил ее покраснеть. Это был голос Элен. Не успела Наташа снять примериваемый лиф, как дверь отворилась и в комнату вошла графиня Безухая, сияющая добродушной и ласковой улыбкой, в темнолиловом, с высоким воротом, бархатном платье.
– Ah, ma delicieuse! [О, моя прелестная!] – сказала она красневшей Наташе. – Charmante! [Очаровательна!] Нет, это ни на что не похоже, мой милый граф, – сказала она вошедшему за ней Илье Андреичу. – Как жить в Москве и никуда не ездить? Нет, я от вас не отстану! Нынче вечером у меня m lle Georges декламирует и соберутся кое кто; и если вы не привезете своих красавиц, которые лучше m lle Georges, то я вас знать не хочу. Мужа нет, он уехал в Тверь, а то бы я его за вами прислала. Непременно приезжайте, непременно, в девятом часу. – Она кивнула головой знакомой модистке, почтительно присевшей ей, и села на кресло подле зеркала, живописно раскинув складки своего бархатного платья. Она не переставала добродушно и весело болтать, беспрестанно восхищаясь красотой Наташи. Она рассмотрела ее платья и похвалила их, похвалилась и своим новым платьем en gaz metallique, [из газа цвета металла,] которое она получила из Парижа и советовала Наташе сделать такое же.
– Впрочем, вам все идет, моя прелестная, – говорила она.
С лица Наташи не сходила улыбка удовольствия. Она чувствовала себя счастливой и расцветающей под похвалами этой милой графини Безуховой, казавшейся ей прежде такой неприступной и важной дамой, и бывшей теперь такой доброй с нею. Наташе стало весело и она чувствовала себя почти влюбленной в эту такую красивую и такую добродушную женщину. Элен с своей стороны искренно восхищалась Наташей и желала повеселить ее. Анатоль просил ее свести его с Наташей, и для этого она приехала к Ростовым. Мысль свести брата с Наташей забавляла ее.
Несмотря на то, что прежде у нее была досада на Наташу за то, что она в Петербурге отбила у нее Бориса, она теперь и не думала об этом, и всей душой, по своему, желала добра Наташе. Уезжая от Ростовых, она отозвала в сторону свою protegee.
– Вчера брат обедал у меня – мы помирали со смеху – ничего не ест и вздыхает по вас, моя прелесть. Il est fou, mais fou amoureux de vous, ma chere. [Он сходит с ума, но сходит с ума от любви к вам, моя милая.]
Наташа багрово покраснела услыхав эти слова.
– Как краснеет, как краснеет, ma delicieuse! [моя прелесть!] – проговорила Элен. – Непременно приезжайте. Si vous aimez quelqu"un, ma delicieuse, ce n"est pas une raison pour se cloitrer. Si meme vous etes promise, je suis sure que votre рromis aurait desire que vous alliez dans le monde en son absence plutot que de deperir d"ennui. [Из того, что вы любите кого нибудь, моя прелестная, никак не следует жить монашенкой. Даже если вы невеста, я уверена, что ваш жених предпочел бы, чтобы вы в его отсутствии выезжали в свет, чем погибали со скуки.]
«Стало быть она знает, что я невеста, стало быть и oни с мужем, с Пьером, с этим справедливым Пьером, думала Наташа, говорили и смеялись про это. Стало быть это ничего». И опять под влиянием Элен то, что прежде представлялось страшным, показалось простым и естественным. «И она такая grande dame, [важная барыня,] такая милая и так видно всей душой любит меня, думала Наташа. И отчего не веселиться?» думала Наташа, удивленными, широко раскрытыми глазами глядя на Элен.
К обеду вернулась Марья Дмитриевна, молчаливая и серьезная, очевидно понесшая поражение у старого князя. Она была еще слишком взволнована от происшедшего столкновения, чтобы быть в силах спокойно рассказать дело. На вопрос графа она отвечала, что всё хорошо и что она завтра расскажет. Узнав о посещении графини Безуховой и приглашении на вечер, Марья Дмитриевна сказала:
– С Безуховой водиться я не люблю и не посоветую; ну, да уж если обещала, поезжай, рассеешься, – прибавила она, обращаясь к Наташе.
Граф Илья Андреич повез своих девиц к графине Безуховой. На вечере было довольно много народу. Но всё общество было почти незнакомо Наташе. Граф Илья Андреич с неудовольствием заметил, что всё это общество состояло преимущественно из мужчин и дам, известных вольностью обращения. M lle Georges, окруженная молодежью, стояла в углу гостиной. Было несколько французов и между ними Метивье, бывший, со времени приезда Элен, домашним человеком у нее. Граф Илья Андреич решился не садиться за карты, не отходить от дочерей и уехать как только кончится представление Georges.
Анатоль очевидно у двери ожидал входа Ростовых. Он, тотчас же поздоровавшись с графом, подошел к Наташе и пошел за ней. Как только Наташа его увидала, тоже как и в театре, чувство тщеславного удовольствия, что она нравится ему и страха от отсутствия нравственных преград между ею и им, охватило ее. Элен радостно приняла Наташу и громко восхищалась ее красотой и туалетом. Вскоре после их приезда, m lle Georges вышла из комнаты, чтобы одеться. В гостиной стали расстанавливать стулья и усаживаться. Анатоль подвинул Наташе стул и хотел сесть подле, но граф, не спускавший глаз с Наташи, сел подле нее. Анатоль сел сзади.
M lle Georges с оголенными, с ямочками, толстыми руками, в красной шали, надетой на одно плечо, вышла в оставленное для нее пустое пространство между кресел и остановилась в ненатуральной позе. Послышался восторженный шопот. M lle Georges строго и мрачно оглянула публику и начала говорить по французски какие то стихи, где речь шла о ее преступной любви к своему сыну. Она местами возвышала голос, местами шептала, торжественно поднимая голову, местами останавливалась и хрипела, выкатывая глаза.
– Adorable, divin, delicieux! [Восхитительно, божественно, чудесно!] – слышалось со всех сторон. Наташа смотрела на толстую Georges, но ничего не слышала, не видела и не понимала ничего из того, что делалось перед ней; она только чувствовала себя опять вполне безвозвратно в том странном, безумном мире, столь далеком от прежнего, в том мире, в котором нельзя было знать, что хорошо, что дурно, что разумно и что безумно. Позади ее сидел Анатоль, и она, чувствуя его близость, испуганно ждала чего то.
После первого монолога всё общество встало и окружило m lle Georges, выражая ей свой восторг.
– Как она хороша! – сказала Наташа отцу, который вместе с другими встал и сквозь толпу подвигался к актрисе.
– Я не нахожу, глядя на вас, – сказал Анатоль, следуя за Наташей. Он сказал это в такое время, когда она одна могла его слышать. – Вы прелестны… с той минуты, как я увидал вас, я не переставал….
– Пойдем, пойдем, Наташа, – сказал граф, возвращаясь за дочерью. – Как хороша!
Наташа ничего не говоря подошла к отцу и вопросительно удивленными глазами смотрела на него.
После нескольких приемов декламации m lle Georges уехала и графиня Безухая попросила общество в залу.
Граф хотел уехать, но Элен умоляла не испортить ее импровизированный бал. Ростовы остались. Анатоль пригласил Наташу на вальс и во время вальса он, пожимая ее стан и руку, сказал ей, что она ravissante [обворожительна] и что он любит ее. Во время экосеза, который она опять танцовала с Курагиным, когда они остались одни, Анатоль ничего не говорил ей и только смотрел на нее. Наташа была в сомнении, не во сне ли она видела то, что он сказал ей во время вальса. В конце первой фигуры он опять пожал ей руку. Наташа подняла на него испуганные глаза, но такое самоуверенно нежное выражение было в его ласковом взгляде и улыбке, что она не могла глядя на него сказать того, что она имела сказать ему. Она опустила глаза.
– Не говорите мне таких вещей, я обручена и люблю другого, – проговорила она быстро… – Она взглянула на него. Анатоль не смутился и не огорчился тем, что она сказала.
– Не говорите мне про это. Что мне зa дело? – сказал он. – Я говорю, что безумно, безумно влюблен в вас. Разве я виноват, что вы восхитительны? Нам начинать.