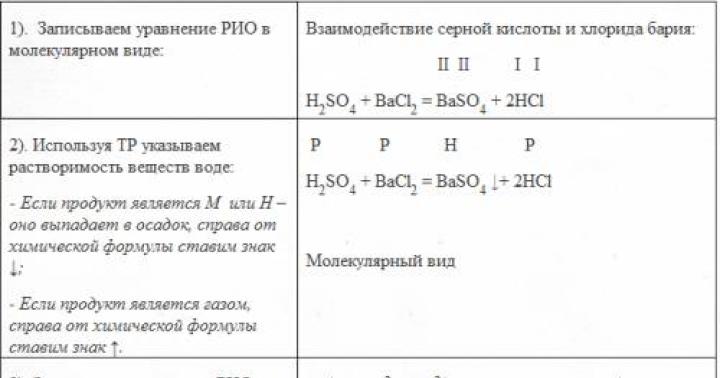
Урок 4 . Анилин как представитель ароматических аминов
Состав и строение, молекулярная и структурная формулы;
Взаимное влияние атомов в молекуле;
Физические свойства;
Химические свойства: реакции анилина по аминогруппе и ароматическому ядру.
Состав и строение, молекулярная и структурная формулы . Анили́н (аминобензол, фениламин) - органическое соединение с формулой C 6 H 5 NH 2 , состоит из бензольного кольца, в котором один атом водорода замещен на аминогруппу. Простейший ароматический амин. Структурная формула:
Впервые анилин получил в 1826 в процессе перегонки индиго с известью немецкий химик, который дал ему название «кристаллины». 1834 Ф. Рунге обнаружил анилин в каменноугольной смоле и назвал «кианолом». 1841 Ю. Ф. Фришце получил анилин в результате нагрева индиго с раствором КОН и назвал его «анилином». 1842 анилин получил М. М. Зинин путем восстановления нитробензола (NH 4) 2 SO 3 и назвал его «бензидамом». 1843 А. В. Гофман установил идентичность всех перечисленных соединений. Слово «анилин» происходит от названия одного из растений, содержащих индиго.
Взаимное влияние атомов в молекуле .
Влияние аминогруппы на свойства бензольного кольца. По отношению к кольцу аминогруппа выступает донором электронов, т.е. нагнетает на кольцо электронную плотность. Эта избыточная плотность в кольце в основном сосредотачивается в положениях 2,4,6 (орто - и ядра-положениях):

В результате: 1) реакции замещения в кольце для анилина протекают легче, чем для бензола; 2) вступающий в кольцо заместитель направляется аминогруппой преимущественно в положения 2,4,6.
Влияние кольца на свойства аминогруппы. Ароматическое кольцо оттягивает часть электронной плотности с атома азота, вовлекая ее в сопряжение с л-системой. Поэтому основные свойства анилина выражены слабее, чем у аммиака и тем более, чем у алифатических аминов. Водный раствор анилина не изменяет окраску индикаторов. В этом и состоит влияние бензольного кольца на свойства аминогруппы.
Изучение среды раствора анилина http://my.mail.ru/mail/ntl0000/video/29154/31055.html?related_deep=1
Физические свойства . Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного тяжелее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит
Физические свойства анилина https://www.youtube.com/watch?v=2c6J-4sNGPc
Химические свойства . Обязательно просмотрите видео .
Химические свойства https://www.youtube.com/watch?v=qQ6zqUXDJdk
Анилин в отличие от бензола легко реагирует с бромной водой с образованием белого нерастворимого в воде осадка 2,4,6-триброманилина:

Аналогично протекает реакция анилина с раствором хлора в СС1 4 , этаноле.
Анилин практически не реагирует с водой (очень слабые основные свойства); основные свойства анилина проявляются в реакциях с сильными минеральными кислотами:

Анилин реагирует с хлорангидридом уксусной кислоты:

При обработке таких солей водными растворами щелочей можно выделить анилин:
Окисление анилина https://www.youtube.com/watch?v=nvxipFGxTRk
Взаимодействие анилина с соляной кислотой https://www.youtube.com/watch?v=VNUTpSaWQ0Q
Бромирование анилина https://www.youtube.com/watch?v=1UPJceDpelY
Пары анилина сгорают в избытке кислорода
4C 6 H 5 –NH 2 + 31O 2 → 24CO 2 + 14H 2 O + 2N 2
Горение анилина https://www.youtube.com/watch?v=cYtCWMczFFs
В разделе на вопрос Анилин-представитель аминов,строение,функциональная группа!? заданный автором Волосок
лучший ответ это Анили́н (фениламин) - органическое соединение с формулой С6H5NH2, простейший ароматический амин. Содержит аминогруппу -NH2. Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного тяжелее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
Для анилина характерны реакции как по аминогруппе, так и по ароматическому кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов. С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок) .
Осн. способ произ-ва анилина-каталитич. восстановление нитробензола водородом в газовой или жидкой фазе. Газофазный процесс осуществляют в трубчатом контактном аппарате при 250-350°С на никель- или медьсодержащем кат
С6Н5NO2 + 3H2 = C6H5NH2 + 2H2O + 443,8кДж/моль
Анилин отделяется от воды расслаиванием и очищается дистилляцией; реакц. вода обезвреживается биохимически. Для получения 1 т анилина расходуется 1,35 т нитробензола, 800 м3 Н2 и 1 кг катализатора.
В жидкой фазе анилин получают при повыш. давлении Н2 (до 1,1 МПа) и 160-170°С на никелевом или палладиевом кат. с одноврем. отгонкой воды и анилина благодаря теплоты р-ции.
Тип урока: урок изучения нового материала на основе имеющихся знаний
Цель урока: Обобщить, расширить и систематизировать знания и понятия учеников по изученному разделу «Амины». Акцентировать внимание на ключевых понятиях темы «Анилин».
Прогнозируемый результат: Знания будут обобщены и систематизированы с целью.
Задачи урока:
Образовательные:
Проверить знания по изученному разделу, закрепить новый материал, углубить знания по теме; обобщить изученный материал; проверить усвоение материала на основе творческих заданий; формировать умения применять полученные знания на практике при выполнении упражнений и решении задач;
Развивающие:
Способствовать становлению умения оценивать товарища и самого себя развивать умение высказывать свою точку зрения, вести аргументированный разговор, делать выводы на основе анализа; помочь учащимся увидеть результаты своего труда; формировать у учащихся умения выделять главное; развивать познавательную активность и творческие способности.
Воспитательные:
Воспитывать активную жизненную позицию, честность, человеческую порядочность; воспитывать в учениках средствами урока уверенность в своих силах; подвести учащихся к выводу о самоценности человеческих качеств.
Ход урока
I Организационно-мотивационный этап (1 мин)
Цель этапа (ожидаемый результат): мотивировать учащихся на активную работу
Задачи этапа: Настроить учащихся на высокий темп урока
Приветствие учащихся на уроке. Сегодня наш урок будет очень насыщенным, и перед нами будет стоять ряд задач.
Но прежде запишите Д-З Слайд 2 Домашнее задание
(запись в дневник)
1. § 52, § 51повторить.
2. § 52, №4-6 письменно, 1-3 устно
I I Целеполагание (1,5 мин)
Цель: Обобщить знания по пройденному разделу «Амины», приобрести знания по теме урока, уметь сравнивать анилин с другими представителями ароматических и с алифатическими аминами
Задачи: Слайд 3 Задачи на уроке
Вспомнить физические и химические свойства аминов; продолжать формировать умение составлять уравнения реакций, характеризующих свойства аминов; познакомиться с особенностями химических процессов по разделу «Анилин»; продолжать учиться видеть причину течения хим. реакций в зависимости от строения молекулы; оценить свою работу на уроке.
III Основная часть. Изучение нового с опорой на известные факты
Строение аминов и анилина
Изучение нового материала на базе имеющихся знаний
Амины — органические производные , в молекуле которого один, два или все три атома замещены углеводородным остатком.
Соответственно обычно выделяют три типа аминов:
первичный амин метиламин
CH3CH2—NH—CH2CH3
вторичный амин диэтиламин
H3CСH2—N—CH2CH3
третичный амин триэтиламин
Для аминов характерна структурная изомерия:
Изомерия углеродного скелета
Изомерия положения функциональной группы
Первичные, вторичные и третичные амины изомерны друг другу (межклассовая изомерия).
Тренинг по изомерии и номенклатуре аминов
Изучение нового материала
Электронное строение анилина
Амины, в которых аминогруппа связана непосредственно связана с ароматическим кольцом, называются ароматическими аминами.
Простейшим представителем этих соединений является аминобензол, или анилин.
Основной отличительной чертой электронного строения аминов является наличие у атома , входящего в функциональную группу, неподеленной электронной пары. Это приводит к тому, что амины проявляют свойства оснований.
Существуют ионы, которые являются продуктом формального замещения на углеводородный радикал всех атомов водорода в ионе аммония.
Эти ионы входят в состав солей, похожих на соли аммония. Они называются четвертичными солями.
Тренинг по изомерии и номенклатуре ароматических аминов
Изучение физических свойств анилина в сравнении с физическими свойствами аминов
Физические свойства аминов и анилина
Простейшие амины (метиламин, диметиламин, триметил-амин) — газообразные вещества. Остальные низшие амины — жидкости, которые хорошо растворяются в воде. Имеют характерный запах, напоминающий запах аммиака.
Первичные и вторичные амины способны образовывать водородные связи. Это приводит к заметному повышению их температур кипения по сравнению с соединениями, имеющими ту же молекулярную массу, но неспособными образовывать водородные связи.
Анилин — маслянистая жидкость, ограниченно растворимая в воде, кипящая при температуре 184 °С.
Русский химик-органик, академик.
открыл (1842) реакцию восстановления ароматических нитросоединений и получил анилин. Доказал, что амины — основания, способные образовывать соли с различными кислотами. Анилин имеет такое большое промышленное значение, что за одну только реакцию имя этого учёного может быть вписано «золотыми буквами в историю химии.
Химические свойства аминов и анилина
Химические свойства аминов определяются в основном наличием у атома азота неподеленной электронной пары.
1. Амины как основания. Атом азота аминогруппы, подобно атому азота в молекуле аммиака, за счет неподеленной пары электронов может образовывать ковалентную связь по донорно-акцепторному механизму, выступая в роли донора. В связи с этим амины, как и аммиак, способны присоединять катион водорода, т. е. выступать в роли основания.
Как вы уже знаете из курса , реакция аммиака с водой приводит к образованию гидроксид-ионов. Раствор аммиака в воде имеет щелочную реакцию. Растворы аминов в воде также дают щелочную реакцию. А вот анилин является более слабым основанием и с взаимодействует неохотно.
Аммиак, реагируя с кислотами, образует соли аммония. Амины также способны вступать в реакцию с кислотами.
Основные свойства алифатических аминов выражены сильнее, чем у аммиака. Это связано с наличием одного и более донорных алкильных заместителей, положительный индуктивный эффект которых повышает электронную плотность на атоме азота. Повышение электронной плотности превращает азот в более сильного донора пары электронов, что повышает его основные свойства.
Так же и анилин в реакциях с кислотами основные свойства, но они менее выражены, чем у алифатических аминов.
В случае ароматических аминов аминогруппа и бензольное кольцо оказывают существенное влияние друг на друга.
Аминогруппа является ориентантом первого рода. Аминогруппа обладает отрицательным индуктивным эффектом и выраженным положительным мезомерным эффектом. Таким образом, реакции электрофильного замещения (бромирование, нитрование) будут приводить к орто - и пара-замещенным продуктам.
Обратим внимание, что в отличие от бензола, который бромируется только в присутствии катализатора — хлорида железа(III), анилин способен реагировать с бромной водой. Это объясняется тем, что аминогруппа, повышая электронную плотность в бензольном кольце (вспомните аналогичное влияние заместителей в молекулах толуола и фенола), активизирует ароматическую систему в реакциях электрофильного замещения. Кроме того, анилин, в отличие от бензола, немного растворим в воде.
Сопряжение п-системы бензольного кольца с неподеленной электронной парой аминогруппы приводит к тому, что анилин является существенно более слабым основанием, чем алифатические амины.
Особенности реакций полного и неполного окисления аминов и анилина, взаимный переход реакций окисления и восстановления показать.
ЗАПИСЫВАЮТСЯ ВСЕ ПРИМЕРЫ УХР, НАЗЫВАЮТСЯ ПРОДУКТЫ (объяснение ведётся в форме эвристической беседы)
Получение аминов и анилина
1. Получение аминов из галогенопроизводных
СН3СН2Вг + NН3 —> СН3СН2NH2 С6Н5Вг + NН3 —> С6Н5NH2
2. Получение первичных аминов восстановлением нитросоединений — алифатических и ароматических. Восстановителем является водород «в момент выделения», который образуется при взаимодействии, например, цинка со щелочью или железа с соляной кислотой.
Применение аминов и анилина
Амины широко применяются для получения лекарств, полимерных материалов. Анилин — важнейшее соединение данного класса (схема), которое используют для производства анилиновых красителей, лекарств (сульфаниламидных препаратов), полимерных материалов (анилиноформальдегидных смол), взрывчатые вещества, ракетное топливо, пестициды.
«Активные» или «реактивные» красители - лучший выбор из анилиновых красителей, существующих на современном рынке. Эта группа красителей превосходно зарекомендовала себя для тканей из волокон растительного происхождения (хлопок, лён, вискоза, конопля, бамбук, бумага, джут и т. д.).
IV Закрепление изученного материала
1. Укажите число у-связей в молекуле метил-фенил-амина:
а) 6; б) 5; в) 7; г) 4.
2. Какие свойства анилина объясняются влиянием фенильного радикала на аминогруппу:
а) анилин вступает в реакции замещения легче, чем бензол;
б) электронная плотность в ароматическом кольце распределена неравномерно;
в) в отличие от аммиака водный раствор анилина не изменяет окраски лакмуса;
г) как основание анилин слабее, чем аммиак?
3. Напишите графические формулы изомерных аминов с общей молекулярной формулой С4Н11N. Назовите эти вещества.
4. а)Из неорганического сырья получите хлоридфенил аммония.
HC1 + KOH спирт +HI +NH3 +HC1
б) Пропанол-2 → ? → ? → ? → ? → ?
5. Найдите массу 19,6%-ного раствора серной кислоты, способного прореагировать с 11,2 л метиламина (н. у.) с образованием средней соли.
6. Смесь фенола и анилина полностью прореагировала с 480 г. бромной воды с w (Вr2) = 3 %. На нейтрализацию продуктов реакции затратили 36,4 см3 раствора NаОН (w = 10%, р=1,2 г/см3). Определите массовые доли веществ в исходной смеси.
7. На нейтрализацию 30 г смеси бензола, фенола и анилина нужно 49,7 мл 17% НС1 (p = 1,0 г/мл). В реакции такого же количества смеси с бромной водой образуется 99,05 г осадка. Найдите массовые доли компонентов в исходной смеси.
V Оценка деятельности класса. Рефлексия.
Строение анилина
Простейший представитель класса ароматических аминов - анилин. Это маслянистая жидкость, немного растворимая в воде (рис. 1).
Рис. 1. Анилин

Некоторые другие ароматические амины (рис. 2):

орто-толуидин 2-нафтиламин 4-аминобифенил
Рис. 2. Ароматические амины
Как отражается на свойствах вещества сочетание бензольного кольца и заместителя, имеющего неподеленную электронную пару? Электронная пара азота втягивается в ароматическую систему (рис. 3):

Рис. 3. Ароматическая система
К чему это приводит?
Основные свойства анилина
Электронная пара анилина «втянута» в общую ароматическую систему, и электронная плотность на азоте анилина понижена. Значит, анилин будет более слабым основанием, чем амины и аммиак. Анилин не меняет окраску лакмуса и фенолфталеина.

Электрофильное замещение в анилине
Повышенная электронная плотность в бензольном кольце (за счет втягивания электронной пары азота) приводит к облегчению электрофильного замещения, особенно в орто - и пара-положениях.
Анилин реагирует с бромной водой, при этом сразу образуется
2,4,6-триброманилин - белый осадок (качественная реакция на анилин и другие аминбензолы).
Вспомним: бензол взаимодействует с бромом только в присутствии катализатора (рис. 4).

Рис. 4. Взаимодействие анилина с бромом
Окисление анилина
Высокая электронная плотность в бензольном кольце облегчает окисление анилина. Анилин обычно окрашен в коричневый цвет из-за того, что часть его окисляется кислородом воздуха даже в нормальных условиях.
Применение анилина и аминов
Из продуктов окисления анилина получают анилиновые красители, отличающиеся стойкостью и яркостью.
Из анилина и аминов получают применяющиеся для местного наркоза анестезин и новокаин; противобактериальное средство стрептоцид; популярное обезболивающее и жаропонижающее средство парацетамол (рис. 5):


Анестезин новокаин
![]()

стрептоцид парацетамол
(пара-аминобензолсульфамид (пара-ацетоаминофенол)
Рис. 5. Производные анилина
Анилин и амины - сырье для производства пластмасс, фотореактивов, взрывчатых веществ. Взрывчатое вещество гексил (гексанитродифениламин) (рис. 6):

Рис. 6. Гексил
Получение анилина и аминов
1. Нагревание галогеналканов с аммиаком или менее замещенными аминами (реакция Гофмана).
СН3Br + NH3 = CH3NH2 + HBr (правильнее CH3NH3Br);
СH3NH2 + CH3Br = (CH3)2NH + HBr (правильнее (CH3)2NH2Br);
(CH3)2NH + CH3Br = (CH3)3N + HBr (правильнее (CH3)3NHBr).
2. Вытеснение аминов из их солей нагреванием со щелочами:
CH3NH3Cl + KOH = CH3NH2- + KCl + H2O.
3. Восстановление нитро соединений (реакция Зинина):
С6Н5NO2 + 3Fe + 6HCl = C6H5NH2 + 3FeCl2 + 2H2O;
С6Н5NO2 + 3H2 С6Н5NH2 + 2H2O.
Подведение итога урока
На данном уроке была рассмотрена тема «Особенности свойств анилина. Получение и применение аминов». На этом занятии вы изучили особенности свойств анилина, обусловленные взаимным влиянием ароматической структуры и атома, присоединённого к ароматическому кольцу. Также рассмотрели способы получения аминов и области их применения.
Список литературы
Рудзитис Г. Е., Фельдман Ф. Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф. Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012. Химия. 10 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В. В. Еремин, Н. Е. Кузьменко, В. В. Лунин, А. А. Дроздов, В. И. Теренин. - М.: Дрофа, 2008. - 463 с. Химия. 11 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В. В. Еремин, Н. Е. Кузьменко, В. В. Лунин, А. А. Дроздов, В. И. Теренин. - М.: Дрофа, 2010. - 462 с. Хомченко Г. П., Хомченко И. Г. Сборник задач по химии для поступающих в вузы. - 4-е изд. - М.: РИА «Новая волна»: Издатель Умеренков, 2012. - 278 с.
Домашнее задание
№№ 5, 8 (с. 14) Рудзитис Г. Е., Фельдман Ф. Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф. Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012. Сравните свойства аминов предельного ряда и анилина. На примере анилина объясните сущность влияния атомов в молекуле.
Органическая химия. Сайт о химии. Интернет-портал promobud.
Вопрос 1.Амины. Их строение и свойства. Получение анилина и применение.
Ответ. Амины-производные аммиака, в молекуле которого атомы водорода (частично или полностью) замещены углеводородными радикалами.
В зависимости от числа радикалов различают амины первичные (с одним радикалом), вторичные (с двумя) и третичные (с тремя).
R-N-H, R 1 -N-R 2 , R 1 -N-R 2 ,
первичный амин вторичный амин третичный амин
Названия аминов производят от названия радикалов, входящих в их молекулы, добавляя окончание –амин˸
CH 3 NH 2 , CH 3 -NH-CH 3 ,
метиламин диметиламин
CH 3 -CH 2 -N-CH 2 -CH 2 -CH 3 .
метилэтилпропиламин
Физические свойства
Простейшие амины – газы, имеющие запах аммиака. Средние амины – жидкости со слабым запахом рыбы, хорошо растворимые в воде. Высшие амины – твёрдые вещества без запаха. В воде нерастворимы.
Химические свойства
Свойства, сходные со свойствами аммиака
Сходства свойств аминов и аммиака объясняется их электронным строением. Молекулы аммиака и аминов содержат атомы азота, имеющий свободную не поделенную пару электронов (точками указаны электроны атома азота)˸
x ‣‣‣ x ‣‣‣ x ‣‣‣ x ‣‣‣
x ‣‣‣ x ‣‣‣ x ‣‣‣ x ‣‣‣
а) Взаимодействие с водой (образуется основание, раствор имеет щелочную реакцию)˸
CH 3 NH 2 + HOH = + OH - .
гидроксид метиламмония
б) Взаимодействие с кислотами (амины обладают основными свойствами˸ они присоединяют протон H +)˸
CH 3 NH 2 + HCI = [ CH 3 NH 3 ]CI.
хлорид метиламмония
Особые свойства˸
1.Окисление (горение на воздухе)˸
4CH 3 NH 2 + 9O 2 = 4CO 2 + 2N 2 + 10H 2 O.
2.Бромирование˸
C 6 H 5 NH 2 + 3Br 2 = C 6 H 2 Br 3 NH 2 ↓ + 3HBr.
2,4,6 - триброманилин
3.Присоединение алкилгалогенидов˸
C 6 H 5 NH 2 + C 2 H 5 CI = + CI - .
Получение анилина
Получение анилина C 6 H 5 NH 2 – восстановление нитросоединения до амина (реакция Зинина,1842 г.)˸
C 6 H 5 NH 2 + 3(NH 4) 2 S = C 6 H 5 NH 2 + 3S+ 6NH 3 + 2H 2 O.
Fe + 2HCI = FeCI 2 + 2H,
атомарный
C 6 H 5 NO 2 + 6H = C 6 H 5 NH 2 + 2H 2 O.
Наиболее перспективен контактный способ - пропускание смеси паров нитробензола и водорода над катализатором˸
C 6 H 5 NO 2 + 3H 2 ═ C 6 H 5 NH 2 + 2H 2 O.
Восстановители˸ (NH 4) 2 S,H 2 , Fe (в виде чугунных стружек) в присутствии HCI.
Применение анилина˸
1.Как сырье в производстве анилиновых красителей.
2.В фармацевтической отрасли промышленности (для получения сульфаниламидных препаратов).
3.В производстве анилинформальдегидных смол.
4. В производстве взрывчатых веществ.
Вопрос 1.Амины. Их строение и свойства. Получение анилина и применение. - понятие и виды. Классификация и особенности категории "Вопрос 1.Амины. Их строение и свойства. Получение анилина и применение." 2015, 2017-2018.