«Редакторы геномов». От «цинковых пальцев» до CRISPR
Появление методов манипулирования генетическим материалом ознаменовало собой настоящую революцию в биологии, биотехнологии и медицине. Направленное вмешательство в геном живых организмов позволило решать широкий спектр задач, начиная от создания модифицированных видов бактерий, растений и животных, обладающих новыми ценными свойствами, и клеточных моделей, необходимых для создания новых лекарств, до разработки методов генотерапии, открывающей перспективы исправления врожденных генетических нарушений
Но чтобы успешно вторгаться в «святая святых» клетки – ее наследственный материал, необходимы технологии, позволяющие расщеплять и соединять молекулы ДНК в заданных участках. Поистине революционный прорыв в этой области произошел всего несколько лет назад, когда на основе механизмов «бактериального иммунитета» был разработан простой метод генетической инженерии CRISPR/Cas, обеспечивающий точное воздействие на заданные участки ДНК. Этот метод открыл принципиально новые возможности для манипуляций на уровне генома высших организмов, позволяя вносить точечные мутации, исправлять, встраивать или удалять фрагменты и даже целые гены.
Чтобы успешно вторгаться в «святая святых» клетки – ее наследственный материал, необходимы технологии, позволяющие расщеплять и соединять молекулы ДНК в заданных участках.
Для этих целей можно использовать рестриктазы – ферменты, способные узнавать определенные короткие нуклеотидные последовательности и расщеплять по ним молекулу ДНК. Для соединения нуклеотидных фрагментов используют ферменты ДНК-лигазы, которые входят в состав природных ферментных комплексов, исправляющих (репарирующих) повреждения в структуре ДНК. «Сшивку» ДНК можно осуществлять также ферментными комплексами системы рекомбинации, благодаря которой происходит обмен гомологичных фрагментов в составе геномных ДНК в процессе образования половых клеток.
Открытие ферментов рестрикции и ДНК-лигаз в 1960-1970-х гг. стало толчком к появлению генетической инженерии: с помощью этих ферментов оказалось возможным расщеплять ДНК на заданные фрагменты и вновь соединять их, формируя новые генетические конструкции. Так получали (и получают сейчас) различные варианты бактериальных и вирусных геномов.
Однако с помощью такого набора инструментов оказалось крайне трудно манипулировать большими сложными геномами высших организмов. Проблема заключалась в том, что ферменты рестрикции могут «узнавать» только относительно короткие последовательности ДНК. Такой специфичности вполне достаточно для работы с короткими ДНК вирусов и бактерий, поскольку в пределах той же бактериальной ДНК конкретные короткие нуклеотидные последовательности встречаются не слишком часто. Поэтому практически всегда можно подобрать рестриктазу, которая расщепит бактериальную ДНК на достаточно небольшой набор фрагментов, из которых можно затем выбрать нужные. Если повезет, то можно будет даже подобрать фермент, который расщепит ДНК в одном, точно определенном месте.
Но специфичности рестриктаз совершенно недостаточно для работы с геномами растений и животных. Такие геномы содержат множество коротких последовательностей нуклеотидов, которые узнаются рестриктазами, поэтому направленное воздействие на один определенный участок становится невозможным. Между тем для решения большого числа важнейших задач биотехнологии и фундаментальной медицины требовались эффективные и точные инструменты для осуществления точечного воздействия на определенные участки ДНК в составах геномов высших организмов, в том числе человека.
Сначала были химеры
Первые попытки создания методов редактирования сложных геномов связаны с конструированием «искусственных ферментов» в виде олигонуклеотидов (коротких нуклеотидных последовательностей), которые могли бы избирательно связываться с определенными последовательностями в структуре целевой ДНК и несли бы на себе химические группы, способные расщеплять ДНК (Кнорре, Власов, 1985). Однако до сих пор эффективных методов расщепления ДНК на такой основе создать не удалось.
Реально работающим подходом оказалось конструирование химерных нуклеаз – сложных белков, содержащих две структурные единицы, одна из которых катализирует расщепление ДНК, а вторая способна избирательно связываться с определенными нуклеотидными последовательностями в составе целевой молекулы, направляя на этот участок действие нуклеазы. Подобные химерные нуклеазы можно «производить» непосредственно в клетке: для этого в нее вносят соответствующие генно-инженерные конструкции (векторы), кодирующие нуклеазы. Такие векторы снабжаются сигналом ядерной локализации – белковой структурой, обеспечивающей поступление конструкции в ядро клетки к геномной ДНК.
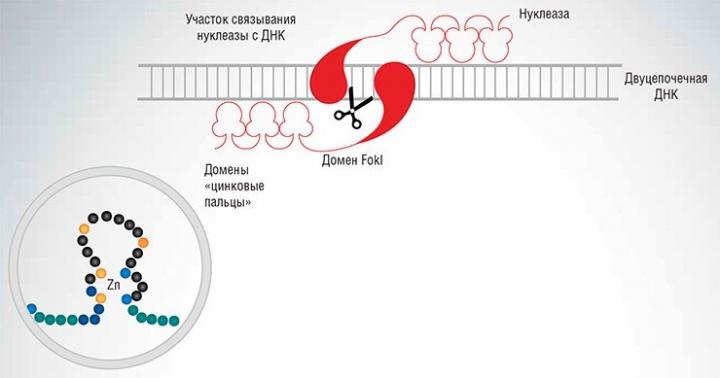
Первыми среди химерных нуклеаз стали zinc-finger нуклеазы, в состав которых в качестве адресующих структур входят так называемые «цинковые пальцы». Последние представляют собой белковые домены (достаточно стабильные и независимые элементы третичной структуры белка), содержащие молекулу цинка и по форме действительно напоминающие палец (Kim et al. , 1996). Каждый «цинковый палец» способен «узнать» и специфично связаться с определенной последовательностью ДНК из трех нуклеотидов.
Нужно сказать, что домены «цинковые пальцы» встречаются в составе человеческих факторов транскрипции – белков, регулирующих процесс синтеза РНК с матрицей ДНК. При создании искусственных нуклеаз можно сконструировать цепочку из «цинковых пальцев» так, что она будет узнавать определенный участок ДНК. Если такая цепочка будет достаточно длинной, она может распознавать относительно протяженные последовательности ДНК, состоящие из ряда тринуклеотидных фрагментов. Это означает реальную возможность точечного воздействия на заданные участки в составе больших сложных геномов.
Однако у метода «цинковых пальцев» обнаружились и серьезные недостатки: во-первых, это не вполне строгое распознавание тринуклеотидных повторов, что приводит к заметному числу расщеплений ДНК в «нецелевых» участках. Во-вторых, метод оказался весьма трудозатратным и дорогостоящим, поскольку для каждой последовательности ДНК необходимо создать свою оптимизированную белковую структуру zinc-finger нуклеазы. Поэтому система «цинковые пальцы» широкого распространения не получила.

Поскольку механизм «узнавания» ДНК в данном случае однозначен и прост (один нуклеотид распознается одним белковым доменом), то получение конструкции, специфично распознающей нужную исследователю нуклеотидную последовательность, – относительно простая задача. Соединяя такую направляющую конструкцию с ферментом, расщепляющим ДНК (как правило, для этих целей используется FokI – каталитический домен фермента рестрикции), мы получаем систему с высокой специфичностью действия.

Здесь нужно отметить, что для успешного разрезания молекулы ДНК с помощью FokI необходимо две субъединицы этого фермента. Поэтому все химерные нуклеазы, в составе которых имеется FokI, работают парами: каждая из них узнает свой специфический участок на разных цепочках молекулы ДНК. Эти целевые сайты выбираются так, чтобы они находились на небольшом (10-20 нуклеотидов) расстоянии, достаточном для димеризации доменов FokI, в результате которой формируется каталитически активная структура. Поскольку каждый из блоков такой бинарной нуклеазы связывается с ДНК независимо, точность расщепления ДНК повышается, а воздействие на «нецелевые» последовательности минимизируется.
Бактериальное ноу-хау
С помощью искусственных нуклеаз TALENs оказалось теоретически возможным внести двунитевой разрыв в любой участок генома. В 2011 г. методы геномной инженерии, в первую очередь использование TALENs, были названы авторитетным журналом «Nature Methods» «методом года» благодаря колоссальному спектру возможных применений в самых разных областях фундаментальной и прикладной науки, от функциональной геномики и биологии развития до сельскохозяйственной биотехнологии.

Однако в 2012-2013 гг. в этой области произошел поистине революционный прорыв: был разработан новый метод генетической инженерии CRISPR/Cas, открывший принципиально новые возможности для манипуляций на уровне генома высших организмов (Cong et al. , 2013). Этот метод чрезвычайно прост, обеспечивает точное воздействие на заданные участки ДНК и может быть использован практически в любой современной молекулярно-биологической лаборатории.
В отличие от химерных нуклеаз, в CRISPR/Cas структурами, узнающими ДНК, являются не белки, а короткие РНК. Идея создания такой системы родилась при изучении механизмов, которые бактерии используют для защиты от своих патогенных вирусов (бактериофагов). Конкретно речь идет о своеобразных «иммунных» реакциях бактерий на проникновение определенного бактериофага, которая выражается в избирательном расщеплении его геномной ДНК.

Работа этого механизма обеспечивается специальными участками бактериального генома – CRISPR локусами (от Clustered Regularly Interspaced Short Palindromic Repeats – короткие палиндромные повторы, регулярно расположенные группами). Как видно по названию, этот локус состоит из стандартных повторенных некодирующих последовательностей бактериальной ДНК, а разделяют эти повторы спейсеры – короткие фрагменты чужеродной (вирусной или плазмидной) ДНК. Последние встраиваются в бактериальный геном после того, как ДНК бактериофага, попавшего в клетку бактерии, рекомбинирует с ее геномом. Состав и порядок расположения спейсеров указывает на число «атак» различных вирусов, успешно пережитых самой бактериальной клеткой и (или) ее родительскими поколениями.
Как это работает? При повторном проникновении в бактериальную клетку уже «известного» ей вируса происходит синтез протяженной первичной РНК, закодированной в CRISPR-локусе. В результате «созревания» этой первичной ДНК образуется ряд коротких фрагментов (crRNA), каждый из которых состоит из специфического участка, соответствующего спейсеру, и универсальных участков, соответствующих палиндромным повторам бактериальной ДНК. Бактериальная ДНК отвечает за привлечение уже упоминавшихся Cas-белков, а спейсер играет роль наводчика: он связывается с определенным, комплементарным ему участком вирусной ДНК, после чего белки Cas разрезают ее, обеспечивая уничтожение бактериофага. Благодаря своей высокой специфичности и способности к быстрой «настройке» система CRISPR/Cas работает очень эффективно, обеспечивая бактерии и ее потомству надежную защиту от патогенов.
К настоящему времени детально описаны несколько типов защитных систем CRISPR, функционирующих в клетках различных бактерий. Наиболее «популярной» оказалась система CRISPR/Cas типа II-А, обнаруженная у бактерии Streptococcus pyogenes , которая состоит из трех генов, кодирующих crRNA, трансактивирующую РНК (tracrRNA) и белок Cas9. На основе этой системы и были созданы универсальные генетические конструкции, кодирующие элементы искусственного «редактора генома» CRISPR/Cas.
Был создан и упрощенный вариант системы, функционирующей в виде комплекса из белка Cas9 и единой направляющей РНК, состоящей из трансактивирующей CRISPR РНК и короткой «зрелой» crRNA. Направляющая последовательность опознает целевой участок ДНК и комплементарно связывается с ним, а Сas9 – разрезает ДНК в нужном месте.
С помощью системы CRISPR/Cas можно осуществлять все виды модификаций генома: вносить точечные мутации, встраивать в определенные места новые гены либо, наоборот, удалять крупные участки нуклеотидных последовательностей, исправлять или заменять отдельные генетические элементы и фрагменты генов.
Технологически стратегия геномной инженерии с помощью системы CRISPR/Cas включает в себя следующие этапы: выбор целевой последовательности и определение вида необходимого воздействия; создание ген-направленной конструкции и доставка ее в клеточное ядро; анализ участка генома, подвергнутого воздействию.

Система CRISPR может быть использована для получения как генетически модифицированных клеток, выращиваемых в культуре, так и живых организмов. В первом случае в клетки вводят плазмиды или вирусные векторы, которые обеспечивают высокий и устойчивый синтез элементов системы CRISPR/Cas. Во втором случае в одноклеточные эмбрионы животных путем микроинъекции вводят уже «готовые» crRNA и мРНК, с которой происходит синтез белка Cas9. Для получения генетически модифицированных растений, клетки которых имеют прочную оболочку, используют выращиваемые в культуре протопласты (растительные клетки без внешней оболочки) и плазмиды, кодирующие элементы CRISPR/Cas. Другой подход, применяемый для растений, – использование агробактерий, природных «генных инженеров», несущих специальную плазмиду.
Настоящее и будущее
Благодаря своей простоте, эффективности и широким возможностям система CRISPR/Cas за короткое время уже нашла применение в самых различных областях фундаментальной и прикладной биологии, биотехнологии и медицины.
Внося модификации в различные элементы генома клеток животных и растений и изучая последствия, ученые получают возможность исследовать роль отдельных генов в функционировании отдельных клеток и всего организма в целом. С помощью системы CRISPR/Cas уже получен ряд мутантных лабораторных животных (мышей, крыс, лягушек, рыб). Все эти модельные организмы открывают новые перспективы для исследований в области биологии развития, иммунологии и изучения заболеваний человека и животных.
Уникальная способность комплекса системы CRISPR/Cas избирательно связываться с определенными участками ДНК позволила разработать на ее основе регуляторы активности генов. Для этого в систему включают каталитически неактивный мутантный белок Cas9, к которому могут быть присоединены белки, активирующие или подавляющие функции промоторов, управляющих работой генов. При связывании такого комплекса с целевой ДНК может подавляться либо стимулироваться работа целевого гена.
Более того, при использовании системы CRISPR/Cas возможно одновременно вводить в клетки несколько генетических конструкций, направленных на разные участки генома. Это позволяет воздействовать на работу одновременно нескольких генов, чтобы исследовать взаимоотношения между ними и их участие в нормальных и патологических процессах жизнедеятельности. Таким способом можно, например, определить мутации в генах, ответственные за развитие устойчивости раковых опухолей к химиотерапии.
Одной из важнейших задач современной биомедицины является создание клеточных моделей для поиска и доклинического исследования новых лекарств. Внося направленные модификации в геном стволовых клеток человека, мы получаем линии клеток-моделей наследственных заболеваний, вызванных нарушениями функций определенных генов. Такие клеточные линии являются, по сути, неограниченным источником «пациентов в пробирке», на которых можно проводить тестирование десятков тысяч различных химических соединений – потенциальных лекарств.
Большие надежды на CRISPR/Cas возлагаются и в связи с развитием генотерапии. Несмотря на многолетние широкие исследования, до настоящего времени не удалось разработать приемлемых методов введения в клетки генов, замещающих дефектные. Главная причина неудач – применение генетических конструкций, содержащих «лишнюю» ДНК (бактериальную или вирусную), к тому же встраивались они неуправляемо, в произвольные участки генома. Все это приводило к различным нарушениям работы генетического аппарата, в том числе к злокачественному перерождению клеток. Однако CRISPR/Cas позволяет вводить гены в геном с хирургической точностью, что делает генотерапию безопасной.
Более того, с помощью этого метода можно не вводить извне «чужие», но редактировать собственный генетический аппарат, сохраняя «свои» системы регуляции. Так уже удалось отредактировать аномальный ген в стволовых клетках пациента, страдающего муковисцидозом (Schwank et al. , 2013). Такие клетки с «отремонтированным» геномом могут быть трансплантированы обратно в организм больного, где они заменят больные клетки и восполнят утраченную ими функцию.
К важнейшим задачам современной биотехнологии и биомедицины, нуждающихся в развитии технологий редактирования геномов, относятся:создание растений и животных, обладающих новыми, ценными свойствами и признаками (урожайность, устойчивость к неблагоприятным условиям среды, вредителям и патогенам);
получение мутантных модельных животных для исследования заболеваний человека;
разработка методов генотерапии, исправления генетических мутаций в культивируемых стволовых клетках человека;
создание клеточных моделей для поиска и доклинического исследования новых лекарств
Применение метода CRISPR/Cas в комбинации с клеточными технологиями открывает принципиальную возможность радикального избавления людей от генетических заболеваний, таких как сахарный диабет, хорея Хантингтона, мышечные дистрофии и др. Генетическое вмешательство может быть осуществлено на уровне эмбрионов, получаемых при проведении экстракорпорального оплодотворения, из которых можно вырастить организм, все клетки которого будут иметь модифицированный геном. Препятствием на пути развития таких технологий являются только этические проблемы: вся необходимая техника уже существует и опробована на лабораторных животных. Например, удалось вырастить здоровых мышей из эмбриональных клеток, в которых был скорректирован дефектный ген, ответственный за развитие катаракты. Эти особи дали здоровое потомство (Wu et al. , 2013).
Современные средства терапии, к сожалению, не способны воздействовать на вирусную ДНК, находящуюся в составе человеческой ДНК. Системы, функционирующие по механизму CRISPR, возможно, позволят в будущем радикально излечивать подобные хронические заболевания, вызываемые вирусами, встраивающимися в геном человека (вирусами гепатита В, герпеса, ВИЧ и др.). Так, известен случай излечения от СПИДа так называемого «берлинского пациента» Т. Брауна в результате пересадки ему стволовых клеток крови от донора, несущего мутацию «невосприимчивости» к ВИЧ. С помощью технологии CRISPR/Cas возможно внести мутацию в этот ген в клетках, которые могут быть затем трансплантированы в организм зараженного.
Одной из важнейших задач современной биотехнологии является создание новых пород скота, а также сельскохозяйственных культур растений, высокоурожайных и устойчивых к неблагоприятным условиям. Главной целью применения метода CRISPR/Cas в биотехнологии является создание генетически модифицированных животных и посевных растений, которые бы обладали новыми ценными свойствами. С помощью этой системы уже внесены точные модификации в геном пшеницы и табака, получены сорта риса, устойчивые к бактериям Xanthomonas , вызывающие бактериальную гниль, которая наносит большой экономический ущерб сельскому хозяйству (Chen, Gao, 2013).
Еще одним интересным биотехнологическим направлением применения системы CRISPR/Cas является получение линий животных или растений, способных синтезировать белки человека, например, инсулин, необходимый больным сахарным диабетом, или альбумин, использующийся при лечении геморрагического шока, ожогов и цирроза печени. Сейчас альбумин получают из плазмы крови человека – весьма ограниченного источника, однако мировая потребность в этом препарате постоянно растет и сегодня составляет 500 т в год. С помощью методов геномной инженерии ген альбумина человека уже введен в геном риса и крупного рогатого скота (He et al. , 2011; Moghaddassi et al. , 2014). Такой белок может быть выделен из растительных и животных тканей, где он синтезировался, и после очищения использован для медицинских целей.
Несомненно, в ближайшее время система CRISPR/Cas будет усовершенствована: можно ожидать упрощения белкового каталитического компонента, повышения избирательности действия системы, создания более эффективных средств доставки в разные типы клеток и целые организмы. Уже получены данные, указывающие на то, что на основе системы CRISPR можно создать средства направленного воздействия не только на ДНК, но и на РНК, что откроет новые возможности для регуляции активности генов и борьбы с вирусными инфекциями.
Хотя система редактирования геномов CRISPR/Cas была создана лишь в 2012 г., она уже применяется во многих лабораториях и компаниях развитых стран. Опубликованы сотни результатов исследований с применением этой технологии, описаны десятки успешных экспериментов по редактированию геномов дрожжей, грызунов, насекомых, растений и человеческих клеток.
Компоненты системы в виде готовых наборов производятся компанией «Life Technologies», недавно слившейся с компанией «Thermo Fisher» (США), и доступны для исследователей. Крупнейшие фармацевтические фирмы, такие как «Takeda», формируют с помощью технологии CRISPR банки генетически модифицированных стволовых клеток – клеточных моделей заболеваний.
Несмотря на активное применение этой технологии в крупных мировых научных центрах, в России CRISPR/Cas используют лишь в нескольких исследовательских центрах, в том числе в Новосибирском Академгородке. Сегодня технологии TALENs и CRISPR/Cas используют в лаборатории эпигенетики развития Института цитологии и генетики СО РАН, лаборатории молекулярной и клеточной медицины Института патологии кровообращения им. академика Е. Н. Мешалкина и в лаборатории стволовых клеток Института химической биологии и фундаментальной медицины СО РАН в работах, связанных с внесением мутаций в стволовые клетки человека, в частности, для создания клеточных моделей бокового амиотрофического склероза, болезни Альцгеймера, Паркинсона и синдрома удлиненного интервала QT.
Однако для проведения полномасштабных исследовательских работ с использованием TALENs и CRISPR/Cas необходимо создание консорциума по клеточным технологиям с привлечением ведущих специалистов на базе профильных НИИ РАМН: кардиологии, иммунологии, неврологии, онкологии и др. Создание в Новосибирском Академгородке Центра клеточных технологий может стать инфраструктурной основой для развития новых биомедицинских технологий и высокотехнологичной фармацевтической промышленности – приоритетных направлений развития научно-технического потенциала страны.
В настоящее время в разработке находится проект Биобанка клеточных моделей заболеваний человека, основой которого станут линии индуцированных плюрипотентных стволовых клеток, полученных из обычных соматических клеток людей, страдающих различными наследственными и приобретенными заболеваниями. Кроме того, в Биобанк войдут клеточные модели наследственных заболеваний человека – клеточные линии, полученные с помощью методов геномной инженерии TALENs и CRISPR/Cas.

Клеточные линии и культуры будут храниться в жидком азоте, – в таком состоянии они могут оставаться жизнеспособными в течение десятилетий и использоваться по мере необходимости. Все хранящиеся в биобанке клеточные культуры и линии будут детально охарактеризованы: для каждой будет составлен «паспорт», содержащий сведения о ее происхождении и характеристиках. Такие клеточные линии могут быть предоставлены в распоряжение как академических институтов для проведения фундаментальных исследований по изучению механизмов развития болезней, так и частным компаниям, занимающимся поиском, разработкой, производством и тестированием новых лекарств.
Литература
Власов В. В. и др. Комплементарные здоровью. Прошлое, настоящее и будущее антисмысловых технологий // НАУКА из первых рук. 2014. № 1 (55). С. 38-50.
Кнорре Д. Г., Власов В. В. // Успехи химии. 1985. T. 54, № 9. С.1420-1447.
Медведев С. П. Как отредактировать наследственность // НАУКА из первых рук. 2014, № 1 (55). С. 10-14.
Сong L., Ran F.A., Cox D. et al. Multiplex genome engineering using CRISPR/Cas systems // Science. 2013, V. 339.
P. 819-823.
Kim Y.G., Cha J., Chandrasegaran, S. (1996). Hybrid restriction enzymes: zinc finger fusions to Fok I cleavage domain. Proc Natl Acad Sci U S A 93, 1156-1160.
Moghaddassi S., Eyestone W., Bishop C.E. (2014). TALEN-mediated modification of the bovine genome for large-scale production of human serum albumin. PLoS One 9, e89631.
Schwank, G., Koo, B.K., Sasselli, V. et al. (2013). Functional repair of CFTR by CRISPR/Cas9 in intestinal stem cell organoids of cystic fibrosis patients. Cell Stem Cell 13, 653-658.
Wu, Y., Liang, D., Wang, Y., Bai, M. et al. Correction of a genetic disease in mouse via use of CRISPR-Cas9. Cell Stem Cell 13, 659-662.
Многие виды миопатий вызваны мутациями в генах. Эти мутации обычными таблетками не исправить, но наука не стоит на месте. В настоящее время учёные разрабатывают различные технологии по редактированию генов.
В этой записи мы собрали некоторые материалы по таким технологиям.
Модификация метода анализа результатов редактирования генома с помощью системы CRISPR/CAS9 на предимплантационных эмбрионах мыши
Аннотация
Генно-модифицированные животные важный инструмент биомедицинских исследований. Для их получения все чаще используют систему редактирования генома CRISPR/Cas9. С помощью микроинъекции комплекс РНК-гида и белка Cas9 доставляется в оплодотворенную яйцеклетку, из которой впоследствии развивается животное с модификацией в геноме. Как правило, анализ специфичности и эффективности системы в каждом случае проводят после получения потомства с вероятной мутацией. Однако анализ на предимплантационной стадии позволил бы сократить время эксперимента, а также понять причину рождения малого числа или даже отсутствия трансгенных особей в потомстве. В статье предложена модификация метода подготовки тотальной ДНК из бластоцист мыши, позволяющая проще и быстрее детектировать результаты микроинъекций комплекса CRISPR/Cas9 в зиготу. Применив описанный в статье метод, мы успешно идентифицировали короткие делеции в интроне 34 гена дистрофина (DMD) в 12 из 13 обработанных эмбрионов и вставку по месту разрыва в интроне 8 гена DMD в 11 из 21 проанализированных образцов. Используя приготовленную предложенным способом тотальную ДНК, можно анализировать до 20 различных сайтов в геноме мышиного эмбриона на стадии бластоцисты, не прибегая к полногеномной амплификации.
Журнал: Вестник Российского государственного медицинского университета, выпуск: № 3 /2016
Технология редактирования генома и возможности ее применения в клеточной нейробиологии
Аннотация
В настоящее время благодаря серии фундаментальных открытий в клеточной и молекулярной биологии появилось несколько высокотехнологичных подходов к моделированию неврологических (в первую очередь нейродегенеративных) заболеваний человека. Среди них направленное геномное редактирование с помощью искусственных нуклеазных систем (CRISPR/CAS9и др.), позволяющее осуществлять высокоспецифичное исправление генетических дефектов на уровне клеток. Особенно перспективным представляется применение технологии геномного редактирования на специализированных нейронах и индуцированных плюрипотентных стволовых клетках (ИПСК), получаемых из фибробластов больных с наследственными формами нейродегенерации в результате клеточного репрограммирования. В статье проводится краткий анализ систем программируемых нуклеаз, рассматриваются механизмы их работы, преимущества, недостатки и возможности применения в моделировании и коррекции нейродегенеративных заболеваний. Обобщен собственный опыт в клеточном моделировании PARK2формы болезни Паркинсона на культуре дофаминергических нейронов, дифференцированных из ИПСК. Представлены предварительные данные, связанные с возможностью редактирования генома клеток в мутантных сайтах PARK2.
Журнал: Анналы клинической и экспериментальной неврологии, выпуск: № 4 / том 9 / 2015
Системы редактирования геномов TALEN и CRISPR/CAS инструменты открытий
Аннотация
Детальное изучение геномов растений, животных и человека открывает широчайшие возможности применения полученных знаний в биотехнологии и медицине. Однако только данных о нуклеотидных последовательностях геномов недостаточно для понимания функциональных взаимосвязей отдельных элементов геномов и их роли в формировании фенотипических признаков и патогенезе отдельных заболеваний. В постгеномную эпоху активно развиваются методы, позволяющие манипулировать с ДНК в геномах, а также визуализировать и управлять экспрессией генов и работой регуляторных элементов. Тем не менее далеко не все методы отвечают высоким требованиям к их эффективности, безопасности и доступности для широкого круга исследователей. В последние несколько лет появились новейшие методы редактирования геномов это системы TALEN (Transcription Activator-Like Effector Nucleases) и CRISPR (Clustered Regulatory Interspaced Short Palindromic Repeats)/Cas9. Эти появившиеся относительно недавно системы уже зарекомендовали себя как эффективные и надежные инструменты геномной инженерии. Данный обзор в основном посвящен применению указанных систем для редактирования геномов основных модельных объектов современной биологии, а также для функционального скрининга геномов, создания клеточных моделей наследственных заболеваний человека, изучения эпигеномов и визуализации клеточных процессов. Кроме того, рассмотрены основные методы конструирования подобных систем, проанализировано их действие, обсуждаются некоторые проблемы, которые ожидают сследователей при применении этих инструментов редактирования геномов.
Журнал: Acta Naturae, выпуск: № 3 (22) / том 6 / 2014
«Редакторы» геномов. От цинковых пальцев до CRISPR
Аннотация
Появление методов манипулирования генетическим материалом ознаменовало собой настоящую революцию в биологии, биотехнологии и медицине. Направленное вмешательство в геном живых организмов позволило решать широкий спектр задач, начиная от создания модифицированных видов бактерий, растений и животных, обладающих новыми ценными свойствами, и клеточных моделей, необходимых для создания новых лекарств, до разработки методов генотерапии, открывающей перспективы исправления врожденных генетических нарушений Но чтобы успешно вторгаться в «святая святых» клетки – ее наследственный материал, необходимы технологии, позволяющие расщеплять и соединять молекулы ДНК в заданных участках. Поистине революционный прорыв в этой области произошел всего несколько лет назад, когда на основе механизмов «бактериального иммунитета» был разработан простой метод генетической инженерии CRISPR/Cas, обеспечивающий точное воздействие на заданные участки ДНК. Этот метод открыл принципиально новые возможности для манипуляций на уровне генома высших организмов, позволяя вносить точечные мутации, исправлять, встраивать или удалять фрагменты и даже целые гены.
Журнал: Наука из первых рук, выпуск: № 2 (56) / 2014
Генно-клеточная терапия наследственных заболеваний мышечной системы: современное состояние вопроса
Аннотация
Генетические заболевания, приводящие к первичному поражению скелетной мышечной ткани, могут быть обусловлены дисфункцией более чем 30 генов. Сегодня не существует эффективных способов их этиотропного и патогенетического лечения. Исследователи сосредотачивают свои усилия на поиске новых терапевтических средств, относящихся к генным и клеточным технологиям, а также использованию малых молекул. В мире проведен большой пул доклинических исследований, а также выполнены несколько десятков клинических исследований. К сожалению, испытанные технологии пока не привели к существенному прогрессу в лечении пациентов с данными заболеваниями. Вместе с тем, полученные данные позволяют определить наиболее целесообразные направления дальнейших разработок – совмещение методик коррекции генома с клеточной доставкой исправленного генома в скелетную мышечную ткань. Настоящий обзор призван дать общие представления об этиологии генетических заболеваний мышц скелета, основных направлениях биотехнологических разработок и результатах выполненных клинических исследований.
Журнал: Гены и клетки, выпуск: № 4 / том 9 / 2014
Как отредактировать наследственность
Аннотация
Второе место в десятке научных прорывов 2013 г., по версии журнала «Science», занял метод редактирования геномов под названием CRISPR/Cas, позволяющий манипулировать хромосомной ДНК прямо в живых клетках. Система CRISPR/Cas состоит из компонентов адаптивной иммунной системы бактерий, адаптированных для работы в клетках высших организмов (эукариот), включая человека. С ее помощью можно не только изучать тяжелые, в том числе наследственные, заболевания, но и создавать модели для разработки новых способов их лекарственной и генной терапии
Журнал: Наука из первых рук, выпуск: № 1 (55) / 2014
Видео TED Talks
Выступления учёных, рассказывающих о технологиях редактирования генов.
Видео на английском языке, но есть возможность включить русские субтитры:
Что вам нужно знать о CRISPR
Возродим ли мы мохнатых мамонтов? Или будем редактировать человеческие эмбрионы? Или сотрём с лица земли целые виды, которые мы расценим как опасные? Технология редактирования генома CRISPR сделала подобные вопросы реальными, но как она работает? Учёный и сторонник научных лабораторий Ellen Jorgensen рассказывает доступным языком о мифах и реальностях CRISPR без пускания пыли в глаза.
Видео выступления:
Как CRISPR позволит нам редактировать ДНК
Генетик Jennifer Doudna – одна их тех, кто разработал новую революционную технологию редактирования генов CRISPR-Cas9. Эта технология позволяет учёным точно редактировать цепочки ДНК, что ведёт к лечению генетических заболеваний… но также и может быть использовано для создания так называемых “дизайнерских детей”. Doudna рассматривает, как CRISPR-Cas9 работает, а также просит научное сообщество сделать паузу и обсудить этическую проблему нового инструмента.
Видео выступления
Генетическое редактирование может изменить целые виды – навсегда
Технология редактирования генов CRISPR позволяет учёным менять последовательности ДНК и гарантирует, что результаты отредактированных генетических особенностей будут наследоваться будущими поколениями, открывая возможность создания альтернативных видов.
Более того, эта технология ведёт нас к вопросам: как новая власть повлияет на человечество? Что мы собираемся менять? Мы теперь боги?
Присоединяйтесь к размышлениям журналиста Jennifer Kahn по поводу данных вопросов.
Запись выступления
Первые трансгенные растения (растения табака со встроенными генами из микроорганизмов) были получены в 1983 г. Первые успешные полевые испытания трансгенных растений (устойчивые к вирусной инфекции растения табака) были проведены в США уже в 1986 г.
После прохождения всех необходимых тестов на токсичность, аллергенность, мутагенность и т.д. первые трансгенные продукты появились в продаже в США в 1994 г. Это были томаты Flavr Savr с замедленным созреванием, созданные фирмой "Calgen", а также гербицид-устойчивая соя компании "Monsanto". Уже через 1-2 года биотехнологические фирмы поставили на рынок целый ряд генетически измененных растений: томатов, кукурузы, картофеля, табака, сои, рапса, кабачков, редиса, хлопчатника.
В настоящее время получением и испытанием генетически модифицированных растений занимаются сотни коммерческих фирм во всем мире с совокупным капиталом более ста миллиардов долларов. В 1999 г. трансгенные растения были высажены на общей площади порядка 40 млн. га, что превышает размеры такой страны, как Великобритания. В США генетически модифицированные растения (GM Crops) составляют сейчас около 50% посевов кукурузы и сои и более 30-40% посевов хлопчатника. Это говорит о том, что генно-инженерная биотехнология растений уже стала важной отраслью производства продовольствия и других полезных продуктов, привлекающей значительные людские ресурсы и финансовые потоки. В ближайшие годы ожидается дальнейшее быстрое увеличение площадей, занятых трансгенными формами культурных растений.
Первая волна трансгенных растений, допущенных для практического применения, содержала дополнительные гены устойчивости (к болезням, гербицидам, вредителям, порче при хранении, стрессам).
Нынешний этап развития генетической инженерии растений получил название "метаболическая инженерия". При этом ставится задача не столько улучшить те или иные имеющиеся качества растения, как при традиционной селекции, сколько научить растение производить совершенно новые соединения, используемые в медицине, химическом производстве и других областях. Этими соединениями могут быть, например, особые жирные кислоты, полезные белки с высоким содержанием незаменимых аминокислот, модифицированные полисахариды, съедобные вакцины, антитела, интерфероны и другие "лекарственные" белки, новые полимеры, не засоряющие окружающую среду и многое, многое другое. Использование трансгенных растений позволяет наладить масштабное и дешевое производство таких веществ и тем самым сделать их более доступными для широкого потребления.
Улучшение качества запасных белков растений
Запасные белки основных культурных видов кодируются семейством близкородственных генов. Накопление запасных белков семян – сложный биосинтетический процесс. Первая генноинженерная попытка улучшения свойства одного растения путем введения гена запасного белка от другого была, проведена Д. Кемпом и Т. Холлом в 1983 г. в США. Ген фазеолина бобов с помощью Ti-плазмиды был перенесен в геном подсолнечника. Результатом этого опыта было лишь химерное растение, получившее название санбин. В клетках подсолнечника были обнаружены иммунологически родственные фазеолиновые полипептиды, что подтверждало факт переноса гена между растениями, относящимися к различным семействам
Позднее ген фазеолина был передан клеткам табака: в растениях-регенерантах ген экспрессировался во всех тканях, хотя и в малых количествах. Неспецифическая экспрессия фазеолинового гена, так же как и в случае переноса его в клетки подсолнечника, сильно отличается от экспрессии этого гена в зрелых семядолях бобов где фазеолин составлял 25-50% от общего белка. Этот факт указывает на необходимость сохранения и других регуляторных сигналов этого гена при конструировании химерных растений и на важность контроля экспрессии генов в процессе онтогенеза растений.
Ген, кодирующий запасной белок кукурузы – зеин, после интеграции его в Т-ДНК был перенесен в геном подсолнечника следующим образом. Штаммы агробактерий, содержащие Ti-плазмиды с геном зеина, использовали для индукции опухолей в стеблях подсолнечника. Некоторые из полученных опухолей содержали мРНК, синтезируемые с генов кукурузы, что дает основание рассматривать эти результаты как первое доказательство транскрипции гена однодольного растения в двудольном. Однако присутствие зеинового белка в тканях подсолнечника не обнаружилось.
Более реальной задачей для генетической инженерии считается улучшение аминокислотного состава белков. Как известно, в запасном белке большинства злаковых наблюдается дефицит лизина, треонина, триптофана, у бобовых - метионина и цистеина. Введение в эти белки дополнительных количеств дефицитных аминокислот могло бы ликвидировать аминокислотный дисбаланс. Методами традиционной селекции удалось существенно повысить содержание лизина в запасных белках злаковых. Во всех этих случаях часть проламинов (спирторастворимые запасные белки злаковых) заменялась другими белками, содержащими много лизина. Однако у таких растении уменьшались размеры зерна и снижалась урожайность. По-видимому, проламины необходимы для формирования нормального зерна, и их замена другими белками отрицательно влияет на урожайность. Учитывая это обстоятельство, для улучшения качества запасного белка зерновых нужен такой белок, который не только отличался бы высоким содержанием лизина и треонина, но и мог полноценно заменить определенную часть проламинов при формировании зерна.
Растения могут производить и белки животного происхождения. Так, встраивание в геном растений Arabidopsis thaliana и Brassica napus химерного гена, состоящего из части гена запасного 25-белка арабидопсиса и кодирующей части для нейропептида - энкефалина, приводило к синтезу химерного белка до 200 нг на 1 г семени. Два структурных белковых домена были связаны последовательностью, узнаваемой трипсином, что давало возможность в дальнейшем легко изолировать чистый энкефалин.
В другом эксперименте удалось после скрещивания трансгенных растений, в одном из которых был встроен ген гамма-субъединицы, а во втором - ген каппа-субъединицы иммуноглобулина, получить у потомства экспрессию обеих цепей. В результате растение формировало антитела, составляющие до 1,3% суммарного белка листьев. Также было показано, что в растениях табака могут собираться полностью функциональные секреторные моноклональные иммуноглобулины. Секреторные иммуноглобулины обычно выделяются в ротовую полость и желудок человека и животных и служат первым барьером на пути кишечных инфекций. В упомянутой выше работе получили продукцию в растениях моноклональных антител, которые были специфичны для Streptococcus mutans - бактерий, вызывающих зубной кариес. Предполагается, что на основе таких моноклональных антител, продуцируемых трансгенными растениями, удастся создать действительно антикариесную зубную пасту. Из других белков животного происхождения, которые представляют интерес для медицины, показана продукция в растениях человеческого β-интерферона.
Разработаны также подходы, позволяющие получать бактериальные антигены в растениях и использовать их в качестве вакцин. Получен картофель, экспрессирующий олигомеры нетоксичной субъединицы β-токсина холеры. Эти трансгенные растения могут быть использованы для получения дешевой вакцины от холеры.
Жиры
Важнейшим сырьем для получения разного рода химических веществ являются жирные кислоты - основной компонент растительного масла. По своей структуре это углеродные цепи, которые обладают различными физико-химическими свойствами в зависимости от своей длины и степени насыщения углеродных связей. В 1995 году была закончена экспериментальная проверка и получено разрешение от федеральных властей США на выращивание и коммерческое использование трансгенных растений рапса с измененным составом растительного масла, включающего вместе с обычными 16- и 18-членными жирными кислотами также и до 45% 12-членной жирной кислоты - лаурата. Это вещество широко используется для производства стиральных порошков, шампуней, косметики.
Экспериментальная работа заключалась в том, что был клонирован ген специфической тиоэстеразы из растения Umbellularia califomica, где содержание лаурата в жире семян достигало 70%. Структурная часть гена этого фермента под контролем промотора-терминатора гена белка, специфического для ранней стадии семяобразования, была встроена в геном рапса и арабидопсиса, что и привело к увеличению содержания лаурата в масле этих растений.
Из других проектов, связанных с изменением состава жирных кислот, можно упомянуть работы, ставящие целью повышение или снижение содержания ненасыщенных жирных кислот в растительном масле. Интересными представляются эксперименты с петрозелиновой кислотой - изомером олеиновой кислоты, где двойная связь находится за шестым углеродным членом. Эта жирная кислота входит в состав масла кориандра и определяет его более высокую температуру плавления (33°С), в то время как при наличии олеиновой кислоты температура плавления составляет только 12°С. Предполагается, что после переноса генов, определяющих синтез петрозелиновой кислоты, в растения - продуценты растительного масла удастся производить диетический маргарин, содержащий ненасыщенную жирную кислоту. Кроме того, из петрозелиновой кислоты очень легко получать лаурат путем окисления озоном. Дальнейшее изучение специфики биохимического синтеза жирных кислот, по-видимому, приведет к возможности управлять этим синтезом с целью получения жирных кислот различной длины и различной степени насыщения, что позволит значительно изменить производство детергентов, косметики, кондитерских изделий, затвердителей, смазочных материалов, лекарств, полимеров, дизельного топлива и многого другого, что связано с использованием углеводородного сырья.
Полисахариды
Проводится работа по созданию трансгенных растений картофеля и других крахмалнакапливающих культур, в которых это вещество будет находиться в основном в виде амилопектина, то есть разветвленной форме крахмала, или же в основном только в виде амилозы, то есть линейных форм крахмала. Раствор амилопектина в воде более жидкий и прозрачный, чем у амилозы, которая при взаимодействии с водой образует ригидный гель. Так, например, крахмал, состоящий в основном из амилопектина, по-видимому, будет иметь спрос на рынке производителей различных питательных смесей, где сейчас в качестве наполнителя используется модифицированный крахмал. Генетической модификации могут подвергаться также геномы пластид и митохондрий. Такие системы позволяют значительно увеличить содержание продукта в трансгенном материале.
Создание гербицидоустойчивых растений
В новых, интенсивных сельскохозяйственных технологиях гербициды применяются очень широко. Это связано с тем. что на смену прежним экологически опасным гербицидам широкого спектра действия, обладающим токсичностью для млекопитающих и длительно сохраняющимся во внешней среде, приходят новые, более совершенные и безопасные соединения. Однако они обладают недостатком - подавляют рост не только сорняков, но и культурных растений Такие высокоэффективные гербициды, как, глифосат, атразины интенсивно изучаются на предмет выявления механизма толерантности к ним некоторых сорняков. Так, на полях, где широко используют атразин, довольно часто появляются атразинустойчивые биотипы у многих видов растении.
Изучение механизма устойчивости к гербицидам с целью получения методами генетической инженерии культурных растений, обладающих этим признаком, включает следующие этапы: выявление биохимических мишеней действия гербицидов в растительной клетке: отбор устойчивых к данному гербициду организмов в качестве источников генов устойчивости: клонирование этих генов: введение их в культурные растения и изучение их функционирования
Существуют четыре принципиально различных механизма, которые могут обеспечивать устойчивость к тем или иным химическим соединениям, включая гербициды: транспортный, элиминирующий, регуляционный и контактный. Транспортный механизм устойчивости заключается в невозможности проникновения гербицида в клетку. При действии элиминирующего механизма устойчивости вещества, попавшие внутрь клетки, могут разрушаться с помощью индуцируемых клеточных факторов, чаще всего деградирующих ферментов, а также подвергаться тому или иному виду модификации, образуя неактивные безвредные для клетки продукты. При регуляционной резистентности белок или фермент клетки, инактивирующийся под действием гербицида, начинает усиленно синтезироваться, ликвидируя таким образом дефицит нужного метаболита в клетке. Контактный механизм устойчивости обеспечивается изменением структуры мишени (белок или фермент), взаимодействием с которым связано повреждающее действие гербицида
Установлено, что признак гербицидоустойчивости является моногенным, то есть признак детерминируется чаще всего одним-единственным геном. Это очень облегчает возможность использования технологии рекомбинантной ДНК для передачи этого признака. Гены, кодирующие те или иные ферменты деструкции и модификации гербицидов, могут быть с успехом использованы для создания гербицидоустойчивых растении методами генетической инженерии.
Традиционные методы селекции создания сортов, устойчивых к гербицидам, очень, длительны и малорезультативны. Наиболее широко применяемый за рубежом гербицид глифосат (коммерческое название Roundup) подавляет синтез важнейших ароматических аминокислот, воздействуя на фермент 5-енолпирувилшикимат-З-фосфатсинтазу (ЕПШФ-синтаза). Известные случаи устойчивости к этому гербициду связаны либо с повышением уровня синтеза этого фермента (регуляционный механизм), либо с возникновением мутантного фермента, нечувствительного к глифосфату (контактный механизм). Из устойчивых к глифосфату растений был выделен ген ЕПШФ-синтазы и поставлен под промотор вируса мозаики цветной капусты. С помощью Ti-плазмиды эта генетическая конструкция была введена в клетки петунии. При наличии одной копии гена в регенерированных из трансформированных клеток растениях синтезировалось фермента в 20 - 40 раз больше, чем в исходных растениях, но устойчивость к глифосфату увеличилась только в 10 раз.
К числу наиболее распространенных гербицидов, используемых при обработке зерновых культур, относится атразин. Он подавляет фотосинтез, связываясь с одним из белков фотосистемы II и прекращая транспорт электронов. Устойчивость к гербициду возникает в результате точечных мутаций в этом пластохинон связывающем белке (замена серина на глицин), вследствие чего он теряет способность взаимодействовать с гербицидом. В ряде случаев удалось осуществить перенос гена мутантного белка в чувствительные к атразину растения с помощью Ti-плазмиды. Интегрированный в хромосому растений ген устойчивости был снабжен сигнальной последовательностью, которая обеспечивала транспорт синтезируемого белка в хлоропласты. Химерные растения проявляли значительную устойчивость к таким концентрациям атразина, которые вызывали гибель контрольных растений с геном белка дикого типа. Некоторые растения способны инактивировать атразин путем отщепления остатка хлора ферментом глутатион-S-трансфераза. Этот же фермент инактивирует и другие родственные гербициды триазинового ряда (пропазин, симазин и др.).
Существуют растения, естественная устойчивость которых к гербицидам основана на детоксикации. Так, устойчивость растений к хлорсульфурону может быть связана с дезактивацией молекулы гербицида путем его гидроксилирования и последующего гликозилирования введенной гидроксильной группы. Создание растений, устойчивых к патогенам и вредителям Устойчивость растений к тем или иным патогенам чаще всего является сложным мультигенным признаком.
Одновременная передача нескольких локусов трудна даже методами генной инженерии, не говоря о классических методах селекции. Более простым является другой путь. Известно, что у устойчивых растений при атаке патогенов изменяется метаболизм. Накапливаются такие соединения, как Н2О2, салициловая кислота, фитоаллексины. Повышенный уровень этих соединений способствует противостоянию растения в борьбе с патогенами.
Вот один из примеров, доказывающий роль салициловой кислоты в иммунном ответе растений. Трансгенные растения табака, которые содержат бактериальный ген, контролирующий синтез салицилат гидролазы (этот фермент разрушает салициловую кислоту), были неспособны к иммунному ответу. Поэтому изменение генно-инженерным путем уровня салициловой кислоты или выработки в растениях в ответ на патоген Н2О2 может быть перспективным для создания устойчивых трансгенных растений.
В фитовирусологии широко известен феномен индуцированной перекрестной устойчивости растений к вирусным инфекциям. Сущность этого явления состоит в том, что заражение растения одним штаммом вируса предотвращает последующую инфекцию этих растений другим вирусным штаммом. Молекулярный механизм подавления вирусной инфекции пока неясен. Показано, что для иммунизации растений достаточно введения отдельных вирусных генов, например генов капсидных белков. Так, ген белка оболочки вируса табачной мозаики перенесли в клетки табака и получили трансгенные растения, у которых 0,1% всех белков листьев был представлен вирусным белком. Значительная часть этих растений при инфицировании вирусом не проявляла никаких симптомов заболевания. Возможно, что синтезирующийся в клетках белок оболочки вируса мешает вирусной РНК нормально функционировать и формировать полноценные вирусные частицы. Установлено, что экспрессия капсидного белка вируса табачной мозаики, вируса мозаики люцерны, вируса огуречной мозаики, Х-вируса картофеля в соответствующих трансгенных растениях (табак, томаты, картофель, огурцы, перцы) обеспечивает высокий уровень их защиты от последующей вирусной инфекции. Причем у трансформированных растений не отмечалось снижения фертильности, нежелательного изменения ростовых и физиологических характеристик исходных экземпляров и их потомства. Полагают, что индуцированная устойчивость растений к вирусам обусловлена особым антивирусным белком, очень похожим на интерферон животных. Представляется возможным методом генетической инженерии усилить экспрессию гена, кодирующего этот белок, путем его амплификации или подстановки под более сильный промотор.
Следует отметить, что использование генетической инженерии для защиты растений от различных патогенных микроорганизмов в значительной мере сдерживается недостаточностью знаний о механизмах защитных реакций растений. Для борьбы с насекомыми-вредителями в растениеводстве используются химические средства - инсектициды. Однако они оказывают вредное влияние на млекопитающих, убивают и полезных насекомых, загрязняют окружающую среду, дороги, и кроме того, насекомые довольно скоро приспосабливаются к ним. Известно более 400 видов насекомых, устойчивых к используемым инсектицидам. Поэтому все большее внимание привлекают биологические средства борьбы, обеспечивающие строгую избирательность действия и отсутствие адаптации вредителей к применяемому биопестициду.
Уже довольно давно известна бактерия Bacillus thuringiensis, продуцирующая белок, являющийся очень токсичным для многих видов насекомых, в то же время безопасный для млекопитающих. Белок (дельта-эндотоксин, CRY-белок) продуцируется различными штаммами В. thuringiensis. Взаимодействие токсина с рецепторами строго специфично, что усложняет подбор комбинации токсин-насекомое. В природе найдено большое количество штаммов В. thuringiensis, чьи токсины действуют только на определенные виды насекомых. Препараты В. thuringiensis в течение десятилетий использовали для контроля насекомых на полях. Безопасность токсина и его составных белков для человека и других млекопитающих полностью доказана. Встраивание гена этого белка в геном растений дает возможность получить трансгенные растения, не поедаемые насекомыми.
Кроме видоспецифичности по действию на насекомых встраивание прокариотических генов дельта-токсинов в геном растений даже под контролем сильных эукариотических промоторов не привело к высокому уровню экспрессии. Предположительно такое явление возникло в связи с тем, что эти бактериальные гены содержат значительно больше адениновых и тиминовых нуклеотидных оснований, чем растительная ДНК. Эта проблема была решена путем создания модифицированных генов, где из природного гена вырезали и добавляли те или иные фрагменты с сохранением доменов, кодирующих активные части дельта-токсина. Так, например, с помощью таких подходов был получен картофель, устойчивый к колорадскому жуку. Получены трансгенные растения табака, способные синтезировать токсин. Такие растения были нечувствительны к гусеницам Manduca sexta. Последние погибали в течение 3 суток контакта с токсинпродуцирующими растениями. Токсинообразование и обусловленная им устойчивость к насекомым передавалась по наследству как доминантный признак.
В настоящее время так называемые Bt-растения (от В. thuringiensis) хлопка и кукурузы занимают основную долю в общем объеме генетически модифицированных растений этих культур, которые выращивают на полях США.
В связи с возможностями генной инженерии конструировать энтомопатогенные растения на основе токсина микробного происхождения еще больший интерес к себе вызывают токсины растительного происхождения. Фитотоксины являются ингибиторами белкового синтеза и осуществляют защитную функцию, направленную против насекомых-вредителей микроорганизмов и вирусов. Лучше всех среди них изучен рицин, синтезируемый в клещевине: его ген клонирован и установлена нуклеотидная последовательность. Однако высокая токсичность рицина для млекопитающих ограничивает генноинженерные работы с ним только техническими культурами, не используемыми в пищу человека и на корм животным. Токсин, вырабатываемый фитолаккой американской, эффективен против вирусов и безвреден для животных. Механизм его действия заключается в инактивации собственных рибосом при проникновении в клетки различного рода патогенов, в том числе фитовирусов. Пораженные клетки некротизируются, предотвращая размножение патогена и его распространение по растению. В настоящее время проводятся исследования по изучению гена этого белка и передаче его в другие растения.
Вирусные болезни широко распространены среди насекомых, поэтому для борьбы с насекомыми-вредителями можно использовать природные вирусы насекомых, препараты которых называют вирусными пестицидами. В отличие от ядохимикатов они обладают узким спектром действия, не убивают полезных насекомых, они быстро разрушаются во внешней среде и не опасны для растений и животных. Наряду с вирусами насекомых используются как биопестициды некоторые грибы, поражающие насекомых-вредителей. Применяемые сейчас биопестициды являются природными штаммами энтомопатогенных вирусов и грибов, однако не исключена возможность создания в будущем методами генетической инженерии новых эффективных биопестицидов.
Повышение устойчивости растений к стрессовым условиям
Растения очень часто подвергаются воздействию различных неблагоприятных факторов окружающей среды: высокие и низкие температуры, недостаток влаги, засоление почв и загазованность среды, недостаток или, напротив, избыток некоторых минеральных веществ и т. д.
Этих факторов множество, поэтому и способы защиты от них многообразны - от физиологических свойств до структурных приспособлений, позволяющих преодолевать их пагубное действие.
Устойчивость растений к тому или иному стрессовому фактору является результатом воздействия множества разных генов, поэтому говорить о полной передаче признаков толерантности от одного вида растения другому генноинженерными методами не приходится. Тем не менее у генетической инженерии имеются определенные возможности для повышения устойчивости растений. Это касается работы с отдельными генами, контролирующими метаболические ответы растений на стрессовые условия, например сверхпродукцию пролина в ответ на осмотический шок, на действие засоления, синтез особых белков в ответ на тепловой шок и т. д. Дальнейшее углубленное изучение физиологической, биохимической и генетической основы ответной реакции растения на условия среды, несомненно, позволит применять методы генетической инженерии для конструирования устойчивых растений.
Пока можно отметить лишь косвенный подход для получения морозоустойчивых растений, основанный на генноинженерных манипуляциях с Pseudomonas syringae. Этот микроорганизм, сосуществующий с растениями, способствует их повреждению ранними заморозками Механизм явления связан с тем, что клетки микроорганизма синтезируют особый белок, локализующийся во внешней мембране и являющийся центром кристаллизации льда. Известно, что формирование льда в воде зависит от веществ, могущих служить центрами образования льда. Белок, вызывающий формирование кристаллов льда в различных частях растения (листья, стебли, корни), является одним из главных факторов, ответственных за повреждение тканей растений, чувствительных к ранним заморозкам. Многочисленные эксперименты в строго контролируемых условиях показали, что стерильные растения не повреждались заморозками вплоть до - 6 - 8° С, тогда как у растений, имеющих соответствующую микрофлору, повреждения возникали уже при температурах - 1,5 - 2° С. Мутанты этих бактерий, потерявшие способность синтезировать белок, вызывающий формирование кристаллов льда, не повышали температуру образования льда, и растения с такой микрофлорой были устойчивы к заморозкам. Штамм таких бактерий, распыленный над клубнями картофеля, конкурировал с обычными бактериями, что приводило к повышению морозоустойчивости растений. Возможно, такие бактерии, созданные с помощью методов генной инженерии и используемые в качестве компонента внешней среды, будут служить для борьбы с заморозками.
Повышение эффективности биологической азотфиксации
Хорошо изучен фермент ответственный за восстановление молекулярного азота до аммония. - нитрогеназа. Структура нитрогеназы одинакова у всех азотфиксирующих организмов. При фиксации азота непременным физиологическим условием является защита нитрогеназы от разрушения под действием кислорода. Лучше всех среди азотфиксаторов изучены ризобии, образующие симбиоз с бобовыми растениями, и свободноживущая бактерия Klebsiella pneumoniae. Установлено, что у этих бактерий за фиксацию азота ответственно 17 генов - так называемых nif-генов. Все эти гены сцеплены друг с другом и расположены в хромосоме между генами ферментов биосинтеза гистидина и генами, определяющими усвоение шикимовой кислоты. У быстрорастущей ризобии nif-гены существуют в форме мегаплазмиды, содержащей 200-300 тысяч пар нуклеотидов.
Среди генов азотфиксации выявлены гены, контролирующие структуру нитрогеназы, белковый фактор, принимающий участие в транспорте электронов, регуляторные гены. Регуляция генов азотфиксации довольно сложна, поэтому генноинженерный перенос азотфиксирующей функции от бактерий непосредственно высшим растениям в настоящее время уже не обсуждается. Как показали эксперименты, даже в самом простом эукариотическом организме - дрожжах не удалось добиться экспрессии nif-генов, хотя они и сохранялись в течение 50 генераций.
Эти опыты показали, что диазотрофность (азот-фиксация) свойственна исключительно прокариотическим организмам, и nif-гены не смогли преодолеть барьер, разделяющий прокариоты и эукариоты, из-за слишком сложной своей структуры и регуляции генами, расположенными вне nif-области. Возможно, более удачным окажется перенос nif-генов с помощью Ti-плазмид в хлоропласты, поскольку механизмы экспрессии генов в хлоропластах и в клетках прокариот близки. В любом случае нитрогеназа должна быть защищена от ингибирующего действия кислорода. Кроме того, фиксация атмосферного азота - очень энергоемкий процесс. Вряд ли растение под влиянием nif-генов может так кардинально изменить свой метаболизм, чтобы создать все эти условия. Хотя не исключено, что в будущем методами генетической инженерии можно будет создать более экономно работающий нитрогеназный комплекс.
Более реально использование генноинженерных методов для решения следующих задач: повышение способности ризобии колонизировать бобовые растения, повышение эффективности фиксации и ассимиляции азота путем воздействия на генетический механизм, создание новых азотфиксирующих микроорганизмов путем введения в них nif-генов, передача способности к симбиозу от бобовых растений к другим.
Первостепенной задачей генетической инженерии для повышения эффективности биологической фиксации азота является создание штаммов ризобии с усиленной азотфиксацией и колонизирующей способностью. Колонизация бобовых растений ризобиями протекает очень медленно, лишь единичные из них дают начало клубенькам. Это происходит потому, что местом инвазии ризобии является только одна небольшая область между точкой роста корня и ближайшим к ней корневым волоском, находящимся на стадии формирования. Все остальные части корня и развившиеся корневые волоски растения нечувствительны к колонизации. В ряде случаев сформировавшиеся клубеньки оказываются неспособными фиксировать азот, что зависит от многих растительных генов (выявлено не менее пяти), в частности от неблагоприятного сочетания двух рецессивных генов.
Традиционными методами генетики и селекции удалось получить лабораторные штаммы ризобий с более высокой колонизирующей способностью. Но они в полевых условиях испытывают конкуренцию со стороны местных штаммов. Повышение их конкурентоспособности, видимо, можно осуществить генноинженерными методами. Повышение эффективности процесса азотфиксации возможно применением генноинженерных приемов, основанных на увеличении копий гена, усилении транскрипции тех генов, продукты которых образуют «узкое» место в каскадном механизме азотфиксации, путем введения более сильных промоторов и т. п. Важно повышение коэффициента полезного действия самой нитро-геназной системы, осуществляющей непосредственное восстановление молекулярного азота в аммиак.
Повышение эффективности фотосинтеза
С4-растения характеризуются высокими темпами роста и скоростью фотосинтеза, у них практически отсутствует видимое фотодыхание. У большинства сельскохозяйственных культур, относящихся к С3-растениям, высокая интенсивность фотодыхания. Фотосинтез и фотодыхание - тесно связанные процессы, в основе которых лежит бифункциональная активность одного и того же ключевого фермента - рибулозобисфосфат-карбоксилазы (РуБФК). РуБФ-карбоксилаза может присоединять не только С02, но и 02, то есть осуществляет реакции карбоксилирования и оксигенирования. При оксигенировании РуБФ образуется фосфогликолат, который служит основным субстратом фотодыхания - процесса выброса С02 на свету, в результате чего теряется часть фотосинтетических продуктов. Низкое фотодыхание у С4-растений объясняется не отсутствием ферментов гликолатного пути, а ограничением оксигеназной реакции, а также реассимиляцией С02 фотодыхания.
Одной из задач, стоящих перед генетической инженерией, является исследование возможности создания РуБФК с преобладающей карбоксилазной активностью.
Получение растений с новыми свойствами
В последние годы ученые используют новый подход для получения трансгенных растений с "antisense RNA" (перевернутой или антисмысловой РНК), который позволяет управлять работой интересуемого гена. В этом случае при конструировании вектора копию ДНК (к-ДНК) встраиваемого гена переворачивают на 180°. В результате в трансгенном растении образуется нормальная молекула мРНК и перевернутая, которая в силу комплементарности нормальной мРНК образует с ней комплекс и закодированный белок не синтезируется.
Такой подход использован для получения трансгенных растений томатов с улучшенным качеством плодов. Вектор включал к-ДНК гена PG, контролирующего синтез полигалактуроназы - фермента, участвующего в разрушении пектина, основного компонента межклеточного пространства растительных тканей. Продукт гена PG синтезируется в период созревания плодов томатов, а увеличение его количества приводит к тому, что томаты становятся более мягкими, что значительно сокращает срок их хранения. Отключение этого гена в трансгенах позволило получить растения томатов с новыми свойствами плодов, которые не только значительно дольше сохранялись, но и сами растения были более устойчивы к грибным заболеваниям.
Такой же подход можно применить для регулирования сроков созревания томатов, а в качестве мишени в этом случае используют ген EFE (ethylene-forming enzyme), продуктом которого является фермент, участвующий в биосинтезе этилена. Этилен - это газообразный гормон, одной из функций которого является контроль за процессом созревания плодов.
Cтратегия антисмысловых конструкций широко применима для модификации экспрессии генов. Эта стратегия используется не только для получения растений с новыми качествами, но и для фундаментальных исследований в генетике растений. Следует упомянуть еще об одном направлении в генной инженерии растений, которое до недавнего времени в основном использовали в фундаментальных исследованиях - для изучения роли гормонов в развитии растений. Суть экспериментов заключалась в получении трансгенных растений с комбинацией определенных бактериальных гормональных генов, например только iaaM или ipt т.д. Эти эксперименты внесли существенный вклад в доказательство роли ауксинов и цитокининов в дифференцировке растений.
В последние годы этот подход стали использовать в практической селекции. Оказалось, что плоды трансгенных растений с геном iaaM, находящимся под промотором гена Def (ген, который экспрессируется только в плодах), являются партенокарпическими, то есть сформировавшимися без опыления. Партенокарпические плоды характеризуются либо полным отсутствием семян, либо очень небольшим их количеством, что позволяет решить проблему "лишних косточек", например в арбузе, цитрусовых и т.д. Уже получены трансгенные растения кабачков, которые в целом не отличаются от контрольных, но практически не содержат семян.
Обезоруженную, лишенную онкогенов Ti-плазмиду ученые активно используют для получения мутаций. Этот метод носит название Т-ДНК-инсерционного мутагенеза. Т-ДНК, встраиваясь в геном растения, выключает ген, в который она встроилась, а по утрате функции можно легко отбирать мутанты (явление сайлесинга – замолкания генов). Этот метод замечателен также тем, что позволяет сразу обнаружить и клонировать соответствующий ген. В настоящее время таким способом получено множество новых мутаций растений и соответствующие гены клонированы. М. А. Раменской на основе Т-ДНК мутагенеза получены растения томатов с неспецифической устойчивостью к фитофторозу. Не менее интересен и другой аспект работ - получены трансгенные растения с измененными декоративными свойствами.
Один из примеров - это получение растений петунии с разноцветными цветками. На очереди голубые розы с геном, контролирующим синтез голубого пигмента, клонированным из дельфиниума.
Во вселенной стратегической компьютерной игры StarCraft внеземная раса зергов примечательна тем, что научилась усваивать генетический материал других организмов и преобразовывать собственные гены, меняясь и адаптируясь к новым условиям. Эта, на первый взгляд, фантастическая идея намного ближе к реальным возможностям живых организмов, чем кажется.
Сегодня мы очень много знаем про ДНК: этой двухцепочечной молекуле посвящено более двух миллионов научных публикаций. Молекулу ДНК можно рассмотреть как текст, написанный с использованием алфавита из четырех букв (нуклеотидов). Совокупность всех нуклеотидов, составляющих хромосомы любого организма, называется геномом. Геном человека насчитывает примерно три миллиарда «букв».
Отдельные участки генома представляют собой обособленные гены - функциональные элементы, которые чаще всего отвечают за синтез конкретных белков. У человека около 20 000 кодирующих белки генов. Белки, как и молекулы ДНК, являются полимерами, но состоят не из нуклеотидов, а из аминокислот. «Алфавит» аминокислот, входящих в состав белков, насчитывает 20 молекул. Зная нуклеотидную последовательность гена, можно точно определить аминокислотную последовательность белка, который он кодирует. Дело в том, что все организмы используют один и тот же (с небольшими вариациями) хорошо изученный генетический код - правила соответствия кодонов (троек нуклеотидов) определенным аминокислотам. Подобная универсальность позволяет генам из одного организма работать в другом организме и при этом производить тот же самый белок.
Естественная инженерия
Один из основных методов генной инженерии растений использует агробактерии и разработанный ими механизм модификации растительных геномов (см. «ПМ» № 10"2005). Гены обитающих в почве агробактерий кодируют специальные белки, способные «протащить» определенную молекулу ДНК в растительную клетку, встроить ее в растительный геном и тем самым заставить растение производить нужные для бактерии питательные вещества. Ученые позаимствовали эту идею и нашли ей применение, заменив нужные бактериям гены на те, которые кодируют белки, необходимые в сельском хозяйстве. Например, Bt-токсины, которые производят почвенные бактерии Bacillus thuringiensis , абсолютно безопасные для млекопитающих и ядовитые для некоторых насекомых, или белки, придающие растению устойчивость к конкретному гербициду.
Обмен генами для бактерий, даже не родственных, - очень распространенное явление. Именно из-за этого микробы, устойчивые к пенициллину, появились уже через несколько лет после начала его массового применения, а в наши дни проблема устойчивости к антибиотикам стала одной из самых тревожных в медицине.
От вирусов к организмам
Естественной «генной инженерией» занимаются не только бактерии, но и вирусы. В геномах многих организмов, включая человека, есть транспозоны - бывшие вирусы, которые давно встроились в ДНК хозяина и, как правило, не принося ему вреда, могут «перескакивать» с одного места в геноме на другое.
Ретровирусы (такие как ВИЧ) умеют встраивать свой генетический материал прямо в геном эукариотических клеток (например, клеток человека). Аденовирусы не встраивают свою генетическую информацию в геномы животных и растений: их гены могут включаться и работать без этого. Эти и другие вирусы активно используются в генной терапии для лечения целого спектра наследственных заболеваний.
Таким образом, естественная генная инженерия очень широко используется в природе и играет огромную роль в адаптации организмов к окружающей среде. Еще важнее то, что все живые организмы постоянно подвергаются генетическим изменениям в результате случайных мутаций. Из этого следует важный вывод: по сути, каждый организм (если не считать клонов) является уникальным и генетически модифицированным по сравнению со своими предками. У него есть как новые мутации, так и новые комбинации существовавших ранее вариантов генов - в геноме любого ребенка обнаруживаются десятки генетических вариантов, которых не было ни у одного из родителей. Кроме возникновения новых мутаций, в ходе полового размножения в каждом поколении возникает новая комбинация уже существующих у родителей генетических вариантов.
Проверено в опытах
Сегодня активно обсуждается безопасность пищевых продуктов, содержащих генетически модифицированные организмы (ГМО). Для продуктов генной инженерии, осуществляемой человеком, намного лучше подходит термин «генетически модернизированные организмы», так как генная инженерия позволяет ускорить те процессы генетических изменений, которые самостоятельно происходят в природе, и направить их в нужное человеку русло. Однако между механизмами генетической модернизации и природными процессами генетической модификации нет никаких существенных различий, поэтому вполне обоснованно можно считать, что производство ГМ-продуктов питания не несет дополнительных рисков.
Однако, как и любая научная гипотеза, безопасность ГМО нуждалась в экспериментальной проверке. Вопреки многочисленным утверждениям противников ГМО, этот вопрос очень и очень тщательно исследуется не первый десяток лет. В этом году в журнале Critical reviews in biotechnology был опубликован обзор почти 1800 научных работ, посвященных изучению безопасности ГМО за последние десять лет. Лишь в трех исследованиях возникли подозрения о негативном влиянии трех конкретных ГМ-сортов, но эти подозрения не оправдались, еще в двух случаях была установлена потенциальная аллергенность ГМ-сортов. Единственный подтвержденный случай касался гена бразильского ореха, встраиваемого в ГМ-сорт сои. Стандартная в таких случаях проверка реакции сыворотки крови людей, страдающих аллергией, на белок нового ГМ-сорта, показала существование опасности, и разработчики отказались от продвижения сорта на рынок.
Кроме того, стоит отдельно упомянуть обзор 2012 года, опубликованный в журнале Food and Chemical Toxicology , в который вошло 12 исследований безопасности употребления ГМО в пищу на нескольких (от двух до пяти) поколениях животных и еще 12 исследований на животных долгосрочного (от трех месяцев до двух лет) потребления ГМО в пищу. Авторы обзора пришли к выводу об отсутствии каких-либо негативных эффектов ГМО (по сравнению с немодернизированными аналогами).
Скандальные разоблачения
Вокруг некоторых работ, якобы показывающих вред отдельных ГМ-сортов растений, возникают курьезы. Типичный пример, который очень любят приводить противники ГМО, - это нашумевшая публикация французского исследователя Сералини в журнале Food and Chemical Toxicology , который утверждал, что ГМ-кукуруза вызывает рак и увеличение смертности крыс. В научной среде работа Сералини вызвала бурные дискуссии, но не потому, что исследователь получил и опубликовал какие-то уникальные данные. Причиной было то, что с научной точки зрения работа была выполнена крайне небрежно и содержала грубые ошибки, заметные с первого взгляда.
Тем не менее представленные Сералини фотографии крыс с крупными опухолями произвели огромное впечатление на общественность. Несмотря на то что его статья не выдержала объективной критики и была отозвана из журнала, ее продолжают цитировать противники ГМО, которых научная сторона вопроса явно не интересует, а фотографии больных крыс до сих пор показывают с экранов.
Научный уровень обсуждения потенциальной опасности ГМО в СМИ и в обществе в целом поражает наивностью. На прилавках магазинов можно встретить крахмал, соль и даже воду «без ГМО». ГМО постоянно путают с консервантами, пестицидами, синтетическими удобрениями и пищевыми добавками, к которым генная инженерия не имеет прямого отношения. От реальных проблем безопасности питания подобные дискуссии уводят в область спекуляций и подмены понятий.
Опасности - настоящие и нет
Впрочем, ни эта статья, ни другие научные работы не пытаются доказать, что ГМО «абсолютно безопасны». На самом деле ни один продукт питания не является абсолютно безопасным, ведь еще Парацельс сказал знаменитую фразу: «Всё есть яд, и ничто не лишено ядовитости; одна лишь доза делает яд незаметным». Даже обычная картошка может вызывать аллергию, а позеленевшая содержит токсичные алкалоиды - соланины.
Может ли как-то измениться работа уже имеющихся генов растения в результате встраивания нового гена? Да, может, но от изменений в работе генов не застрахован ни один организм. Может ли в результате генной инженерии появиться новый сорт растения, который распространится за пределы сельскохозяйственных угодий и как-то повлияет на экосистему? Теоретически и такое возможно, но и это происходит в природе повсеместно: появляются новые виды, экосистемы меняются, одни виды вымирают, другие занимают их место. Однако нет оснований полагать, что генная инженерия несет в себе дополнительные риски для окружающей среды или для здоровья людей или животных. Но про эти риски постоянно трубят в СМИ. Почему?
Рынок ГМО в значительной степени монополизирован. Среди гигантов на первом месте стоит компания Monsanto. Разумеется, крупные производители ГМ-семян и технологий заинтересованы в прибыли, у них есть собственные интересы и собственное лобби. Но они зарабатывают деньги не «из воздуха», а предлагая человечеству прогрессивные сельскохозяйственные технологии, за которые производители голосуют самым убедительным образом - долларом, песо, юанем и т. д.
Основные производители и поставщики «органических» продуктов, выращенных с использованием устаревших технологий и, следовательно, более дорогих (но не более качественных) - тоже вовсе не мелкие фермеры, а такие же крупные компании с многомиллиардными оборотами. Только в США рынок органических продуктов составил в 2012 году $31 млрд. Это серьезный бизнес, и, поскольку органик-продукты не имеют каких-либо преимуществ перед ГМО, но обходятся дороже в производстве, рыночными методами конкурировать с ГМ-сортами они не могут. Вот и приходится посредством СМИ внушать доверчивым потребителям ничем не обоснованный страх перед мифическими «генами скорпиона», который и рождает спрос на дорогие и нетехнологичные «органик-продукты». Кроме того, противники ГМО, описывающие страшные опасности генно-модифицированных сортов, вырабатывающих белок B. thuringiensis , обычно забывают упомянуть о том, что препараты на основе таких культур или выделенных из них белков в «органическом земледелии» разрешены (и широко применяются). Как и натуральный навоз, который может оказаться источником кучи патогенных бактерий и прочей натуральной гадости.
Немного политики
Сегодня генная инженерия - одна из наиболее изученных с точки зрения безопасности технологий. Она позволяет создавать более качественные продукты питания, уменьшить количество используемых на полях пестицидов и защитить окружающую среду (да, именно защитить: на полях, засеянных Bt-сортами, живет больше насекомых и птиц, чем на «обычных», которые приходится регулярно обрабатывать инсектицидами).
Но существует и еще одна причина «борьбы» с ГМО - исключительно политическая. Страны, значительно отставшие в сфере биотехнологий, пытаются найти повод не допустить более дешевые продукты из других стран на свой рынок. Впрочем, такая защита отечественных производителей от иностранной продукции имеет смысл только в том случае, если помогает выиграть время, чтобы развить собственные технологии до конкурентоспособного состояния. Если же этого не делать, есть серьезный риск отстать от мирового научного и технологического уровня. Навсегда.
НАУЧНАЯ БИБЛИОТЕКА - РЕФЕРАТЫ - Генная модификация
Генная модификация
Генетики и селекционеры обсуждают сложнейшие проблемы селекции растений и животных, применения генетических технологий в медицине, безопасности генетически модифицированных продуктов.
1. Генная инженерия
Генная инженерия - это раздел молекулярной генетики, связанный с целенаправленным созданием новых комбинаций генетического материала. Основа прикладной генной инженерии - теория гена. Созданный генетический материал способен размножаться в клетке-хозяине и синтезировать конечные продукты обмена.
Генная инженерия возникла в 1972 году, в Станфордском университете, в США. Тогда лаборатория П. Берга получила первую рекомбинатную (гибридную) ДНК или (рекДНК). Она соединяла в себе фрагменты ДНК фага лямбда, кишечной палочки и обезьяньего вируса SV40.
Строение рекомбинантной ДНК. Гибридная ДНК имеет вид кольца. Она содержит ген (или гены) и вектор. Вектор - это фрагмент ДНК, обеспечивающий размножение гибридной ДНК и синтез конечных продуктов деятельности генетической системы - белков. Большая часть векторов получена на основе фага лямбда, из плазмид, вирусов SV40, полиомы, дрожжей и др. бактерий.
Синтез белков происходит в клетке-хозяине. Наиболее часто в качестве клетки-хозяина используют кишечную палочку, однако применяют и др. бактерии, дрожжи, животные или растительные клетки. Система вектор-хозяин не может быть произвольной: вектор подгоняется к клетке-хозяину. Выбор вектора зависит от видовой специфичности и целей исследования.
Ключевое значение в конструировании гибридной ДНК несут два фермента. Первый - рестриктаза - рассекает молекулу ДНК на фрагменты по строго определенным местам. И второй - ДНК-лигазы - сшивают фрагменты ДНК в единое целое. Только после выделения таких ферментов создание искусственных генетических структур стало технически выполнимой задачей.
Этапы генного синтеза . Гены, подлежащие клонированию, могут быть получены в составе фрагментов путем механического или рестриктазного дробления тотальной ДНК. Но структурные гены, как правило, приходится либо синтезировать химико-биологическим путем, либо получать в виде ДНК-копии информационных РНК, соответствующих избранному гену. Структурные гены содержат только кодированную запись конечного продукта (белка, РНК), и полностью лишены регуляторных участков. И поэтому эти гены не способны функционировать в клетке-хозяине.
При получении рекДНК образуется чаще всего несколько структур, из которых только одна является нужной. Поэтому обязательный этап составляет селекция и молекулярное клонирование рекДНК, введенной путем трансформации в клетку-хозяина.
Существует 3 пути селекции рекДНК: генетический, иммунохимический и гибризационный с мечеными ДНК и РНК.
В результате интенсивного развития методов генной инженерии получены клоны множества генов: рибосомальной, транспортной и 5S РНК, гистонов, глобина мыши, кролика, человека, коллагена, овальбумина, инсулина человека и др. пептидных гормонов, интерферона человека и прочее. Это позволило создавать штаммы бактерий, производящих многие биологически активные вещества, используемые в медицине, сельском хозяйстве и микробиологической промышленности.
На основе генной инженерии возникла отрасль фармацевтической промышленности, названная "индустрией ДНК". Это одна из современных ветвей биотехнологии .
Нет сомнений, что поиски генетиков сулят человеку избавление от многих недугов . Уже сейчас генная инженерия начинает активно применяться в онкологии, создаются препараты, прицельно направленные против конкретной опухоли. Ученым удалось идентифицировать гены, предрасполагающие к развитию сахарного диабета, - значит, появились новые перспективы в лечении и этого тяжкого недуга. Для лечебного применения допущен инсулин человека (хумулин), полученный посредством рекДНК. Кроме того, на основе многочисленных мутантов по отдельным генам, получаемых при их изучении, созданы высокоэффективные тест-системы для выявления генетической активности факторов среды, в том числе для выявления канцерогенных соединений.
За короткий срок генная инженерия оказала огромное влияние на развитие молекулярно-генетических методов и позволила существенно продвинуться по пути познания строения и функционирования генетического аппарата. Генная инженерия имеет большие перспективы в лечении наследственных болезней, которых на сегодняшний день зарегистрировано около 2000. Генная инженерия призвана помогать исправлять ошибки природы.
С другой стороны, генетические технологии породили совершенно новые проблемы, связанные с возможностью клонирования живых существ, в том числе и человека. Мировое научное сообщество признает, что технически клонирование идентичной человеческой особи становится возможным. Но вопрос о том, нужны ли человечеству подобные попытки, остается открытым. Доказано, что в 99 процентах случаев есть риск врожденных уродств - а значит, такие опыты над человеком недопустимы.
Однако, новые генетические технологии на основе трансгенеза и клонирования играют важнейшую роль в создании высокопродуктивных сортов растений и пород животных. При этом на первый план выходят проблемы, как генетической безопасности, так и морально-правовые .
В России все исследования по клонированию проводятся только на животных. Яростные дискуссии ведутся во всем мире - в том числе и в России - вокруг другого порождения современной науки: генетически модифицированных продуктов .
2. Безопасна ли генная модификация?
Создатели генетически измененных продуктов утверждают, что они совершенно безопасны. Сторонники их широкого использования уверены, что многолетние исследования доказали безвредность такой продукции. Противники убеждены в обратном.
До сих пор не доказано, что эти продукты безопасны для человека. Многие виды генетически модифицированных продуктов запрещаются к использованию на последних стадиях эксперимента как сильные аллергены.
Правы ли скептики, утверждающие, что трансгенные продукты опасны? А может, они станут нашей пищей в 21 веке?
Около 30 лет назад были произведены первые опыты по генетической модификации растений. Например, можно взять один ген от одного животного или растения и вживить его в другое животное или растение. Таким способом, например, можно получить картофель, устойчивый к пестицидам .
Генетически модифицированные продукты не только созданы, но их активно употребляют в пищу.
В традиционной селекции происходит скрещивание внутри одного вида. Даже помидор был улучшен селекцией. Но, при селекции происходит обмен между особями одного вида. А генная инженерия позволяет составить новую ДНК и манипулировать ею. Например, если ген светлячка вставить в ДНК табака, то цветок табака начинает светиться, если нуждается в поливе. Селекционными методами этого не возможно добиться!
Протестующие больше всего обращают внимание на негативные процессы этой методики. Но ведь, никто не спорит с тем, что генетически модифицированные продукты нуждается в тестировании!
Защитники индустрии биотехнологий утверждают, что все процессы, касающиеся генно-модифицированных продуктов, находятся под жестким контролем.
Проводится анализ обыкновенного и трансгенного растения. Ученые должны доказать инспекторам, что пищевые продукты не отличаются по качеству.
Проверка продукта проходит следующие этапы:
1. Сравнение структуры и химического состава обыкновенного и траснсгенного растения.
2. Требуются доказательства того, что употребление нового продукта в пищу не вредит здоровью человека.
Трансгенная соя (обладает устойчивостью к гербицидам) входит в продукты, которые мы употребляем в пищу последние годы.
Токсичен ли новый белок? Несколько лет проводили тестирование белка на токсичность. Кормили мышей дозами в 1000 раз, превышающие дозы, которые потребляет человек. Ученые утверждают, что ничего вредного для организма человека не было выявлено.
Как новые белки перевариваются? Белки, созданные искусственно погружают в раствор, который имеет среду сходную по составу с кишечником. Чем быстрее переваривается продукт, тем лучше.
Эксперименты показали, что новый белок не является аллергеном. Есть и другие способы проверить созданный белок. Если он не проходит проверку, то его уничтожают. Однако, белок трансгенной сои успешно выдержал испытания! Было проведено 1800 анализов, которые показали, что с соевыми бобами все в порядке.
Система тестов работает. Нужно только следовать методике, считают ученые.
Но скептики полагают, что наука знает еще слишком мало, чтобы утверждать, что “все под контролем”. Живые организмы настолько сложны, что предвидеть их поведение практически невозможно.
Однако, традиционные методы селекции не всегда безопасны . Напротив, в генной инженерии точно известны пути внедрения гена. Опять же, скептики уверены, в том, что генная инженерия, использующая новые методы, рискует нанести непоправимый вред природе. Их противники, говорят, что и селекция опасна, т.к. она имеет дело не с одним, а с несколькими генами! А потому результат селекции еще более непредсказуем!
Страшнее всего, то, что лет 30 тому назад экспериментировали с генами, не понимая, что делают!
Сопротивление генно-модифицированной продукции в Европе сильнее, чем где-либо еще в мире. Последнее время внедрение трансгенных продуктов очень затруднено: в Англии таковых продуктов было внедрено около 2000, а теперь осталось меньше 100!
3. Примеры генной модификации
Общественные организации в Европе призывают уничтожать трансгенные растения. Странные растения получают, вживляя в них гены животных. Экологи против этих технологий, общественность высокомерно и презрительно относится к генетически модифицированным продуктам.
3.1 Увеличение початка кукурузы
В Мексике - бедные почвы, а потому очень плохие урожаи кукурузы. Ученым поставлена задача, по увеличению размера початка кукурузы . В результате проведенных исследований, вживили в кукурузу ген, который нейтрализует соли алюминия и растворяет фосфаты, это позволило растению полноценно развиваться на предлагаемых почвах.
Урожай обещал быть в 2 раза больше, но правительство под давлением экологических организаций запретило заниматься этими исследованиями. Экологи игнорируют результаты эксперимента. Противники генной инженерии считают, что такие опыты наносят вред экологии, опасны для здоровья и в конечном итоге приводят к экологической катастрофе. Ведь, никто не даст гарантии, что эти методики не приведут к появлению новых насекомых и сорняков!
3.2 Защита хлопчатника
Университет Аризоны. Ученые работают над увеличением урожайности хлопка. Растение страдает от нашествия розового коробчатого червя. Если популяция вредителя большая, то урожаи хлопка стремительно падают!
Требуется внедрить в хлопчатник такой ген, который будет убивать коробчатого червя. Последние 40 лет для уничтожения насекомых применяли опрыскивание растений химикатами. Страдали и люди, и животные. Попробовали вживить в хлопок ген бактерии. В листьях растения появился белок, который ядовит для червя. Таким образом, необходимость защиты растения химикатами отпадает!
В результате получили сотни гектаров ядовитых растений, которые сами защищаются от вредных насекомых. Опять же, пройдет время, и вредители привыкнут, выработают иммунитет!
Но не только жуки - вредители внушают опасения! Экологи боятся, что появятся особо устойчивые сорняки, и, значит, не будет спасения от сорняков устойчивых к химикатам. Ведь пчелы могут разнести пыльцу на несколько километров, и эти растения заполнят всю округу. Однако, есть данные, что на расстоянии 15 м опыление уже не происходит. Но если даже пыльца модифицированного растения преодолеет расстояние, то она должна скрестится со своим видом. Сверхживучесть сохранить не так просто…
3.3 Рис с витамином “А”
Азия. 100 млн. детей не получают витамин “А”, который необходим для полноценного зрения. Дело в том, что основная пища беднейших слоев населения – рис. Дети слепнут от недостатка витамина “А”!
Благородная задача - вырастить рис сразу с витамином “А” и засеять им поля в отсталых странах. Как это возможно? Нарцисс – ядовитое растение. Из него необходимо взять 2 гена и внедрить в рис, который в таком случае будет содержать витамин “А”!
4. Ужасы генной модификации
Ген человеческой печени добавляют в рис! Ученые начали добавлять человеческие гены в рис в попытке поднять генно-модифицированные продукты на новый уровень.
Исследователи ввели в рис ген, полученный из печени человека, производящий энзим, способствующий распаду вредных химических элементов в организме человека. Они надеются, что энзим – CYP2B6 – сделает то же самое с гербицидами и загрязняющими веществами, будучи смешанным с рисом.
Однако противники генно-модифицированных продуктов говорят, что использование человеческих генов отпугнет потребителей, которым претит идея каннибализма и того, что ученые берут на себя функции бога. Сью Майер из британской организации GeneWatch говорит: "Я не думаю, что кто-то захочет купить этот рис". "Люди уже выразили свое отвращение по поводу использования человеческих генов и беспокойство в связи с ощущением, что индустрия биотехнологий не прислушивается к ним. Это еще больше пошатнет их уверенность".
Обычно при генной модификации зерновых культур используются гены, полученные из бактерий. Они устойчивы только к одному виду гербицидов, что означает, что фермеры могут обрабатывать свои поля как угодно часто для борьбы с вредителями, но только одним видом химикатов. Цель добавления в рис человеческого гена – создать растение, устойчивое к нескольким видам гербицидов.
Исследователи в Национальном институте агробиологических наук в Цукубе в Японии обнаружили, что новый вид риса может быть устойчивым к 14 различным видам гербицидов. Профессор Ричард Мейлан, проводивший подобные исследования в Институте Пердью в Индиане говорит, что такой рис можно выращивать на почве, пропитанной промышленными загрязнениями. Он применял в своих исследованиях гены кроликов, но говорит, что не видит причин, по которым нельзя использовать человеческие гены. Он говорит, что разговоры о "пище Франкенштейна" – это чепуха, и добавляет: "Я не думаю, что этические соображения имеют какое-то отношение к использованию человеческих генов в генной инженерии при выращивании продуктов".
Производство риса во всем мире падает, и идет гонка в поисках путей повышения сборов риса, а также новых разновидностей риса, устойчивых к вирусам, с низким содержанием аллергенов и белка.
Однако в Институте Науки в обществе противников генной модификации говорят, что энзим CYP2B6 может ударить по человеку, приведя к созданию новых вирусов или разновидностей рака.
Они добавляют: "Сторонники генной модификации и страны, являющиеся основными производителями риса, исследуют и продвигают генно-модифицированный рис, совершенно не задумываясь о безопасности и долговременной перспективе" .
Заключение
Скептики не уверены, что генные технологии решат социальные проблемы. Мечты о равном распределении продуктов питания по всему миру – утопия.
Сопротивление генно-модифицированной продукции в Европе сильнее, чем где-либо еще в мире. Создатели генетически измененных продуктов утверждают, что они совершенно безопасны. В свою очередь, противники генной модификации считают ее "ящиком Пандоры" с непредсказуемыми последствиями.
Очевидно, что в ближайшие десятилетия генетика еще преподнесет человечеству немало сюрпризов, породит множество сенсаций - мнимых и реальных, вокруг нее будут бушевать споры и даже скандалы. Общество легко слышит тех людей, которые боятся всего нового, но опасность от мобильных телефонов не меньше!
Главное, чтобы вся эта суета не слишком мешала серьезной работе ученых на одном из самых интересных и перспективных научных направлений.
Терминологический словарь
Генная инженерия - практика целенаправленного изменения генетических программ половых клеток с целью придания исходным формам организмов новых свойств или создания принципиально новых форм организмов. Основной метод генной инженерии состоит в извлечении из клеток организма гена или группы генов, соединение их с определенными молекулами нуклеиновых кислот и внедрение полученных гибридных молекул в клетки другого организма.
Биологическая защита - в генной инженерии - создание и использование безопасной для человека и объектов окружающей среды комбинации биологического материала, свойства которого исключают нежелательное выживание генно-инженерно-модифицированных организмов в окружающей среде и/или передачу им генетической информации
Биотехнология Biotechnology - в широком смысле - пограничная между биологией и техникой научная дисциплина и сфера практики, изучающая пути и методы изменения окружающей человека природной среды в соответствии с его потребностями.
Биотехнология - в узком смысле - совокупность методов и приемов получения полезных для человека продуктов и явлений с помощью биологических агентов. В состав биотехнологии входят генная, клеточная и экологическая инженерии
Выпуск генно-инженерно-модифицированных организмов в окружающую среду - действие или бездействие, в результате которых произошло внесение генно-инженерно-модифицированных организмов в окружающую среду.
Генно-инженерная деятельность - деятельность, осуществляемая с использованием методов генной инженерии и генно-инженерно-модифицированных организмов.
Генно-инженерно-модифицированный организм - организм или несколько организмов, любое неклеточное, одноклеточное или многоклеточное образование: - способное к воспроизводству или передаче наследственного генетического материала; - отличное от природных организмов; - полученное с применением методов генной инженерии; и - содержащее генноинженерный материал.
Генодиагностика - в генной инженерии - совокупность методов по выявлению изменений в структуре генома.
Замкнутая система - в генной инженерии - система осуществления генно-инженерной деятельности, при которой генетические модификации вносятся в организм или генно-инженерно-модифицированные организмы, обрабатываются, культивируются, хранятся, используются, подвергаются транспортировке, уничтожению или захоронению в условиях существования физических, химических и биологических барьеров или их комбинаций, предотвращающих контакт генно-инженерно-модифицированных организмов с населением и окружающей средой.
Открытая система - в генной инженерии - система осуществления генно-инженерной деятельности, предполагающая контакт генно-инженерно-модифицированных организмов с населением и окружающей средой при их намеренном выпуске в окружающую среду, применении в медицинских целях, при экспорте и импорте, при передаче технологий.
Трансгенные организмы - животные, растения, микроорганизмы, вирусы, генетическая программа которых изменена с использованием методов генной инженерии.
Физическая защита - в генной инженерии - создание и использование специальных технических средств и приемов, предотвращающих выпуск генно-инженерно-модифицированных организмов в окружающую среду и/или передачу им генетической информации.
Литература
1.Маниатис Т., Методы генетической инженерии, М., 1984;
2.Генная инженерия Источник #"#">#"#">Рубрикон
Генно-инженерно-модифицированный организм - организм или несколько организмов, любое неклеточное, одноклеточное или многоклеточное образование: - способное к воспроизводству или передаче наследственного генетического материала; - отличное от природных организмов; - полученное с применением методов генной инженерии; и - содержащее генно-инженерный материал.
Фаги, то же, что бактериофаги. …фаг (от греч. Phagos –пожиратель) часть сложных слов, соответствующая по значению словам ”поедающий’, ‘поглощающий” (например, бактериофаг).
Биотехнология- совокупность методов и приемов получения полезных для человека продуктов и явлений с помощью биологических агентов. В состав биотехнологии входят генная, клеточная и экологическая инженерии.
Генетики вывели соевые бобы, предотвращающие потерю волос. В Японии выведен генетически измененный сорт соевых бобов, которые стимулируют рост волос и предотвращают их потерю от химиотерапии. Если подтвердится безопасность нового продукта, то, чтобы спастись от облысения, нужно будет просто периодически есть эти бобы, сообщил в среду глава исследовательской группы Университета Киото профессор Массаки Иосикава. Чудодейственное свойство зерновой культуре придал генетически внедренный компонент (новокинин), обладающий противогипертоническим эффектом. Он был получен из аминокислотного состава яичного белка. По словам ученых, этот компонент способствует росту волос тем, что расширяет сосуды и нормализует циркуляцию крови. Эффективность бобов подтверждена в ходе экспериментов над мышами, которых побрили, а затем кормили модифицированными бобами из расчета одна тысячная миллиграмма противогипертонического вещества на грамм массы тела. Как сообщается, восстановление шерстяного покрова шло ускоренными темпами, а после увеличения дозы мыши переставали терять шерсть даже в результате химиотерапии. Специалисты говорят, что их бобы также можно использовать в качестве обычного лекарства от высокого давления. 13 Апреля 2005